過硫酸カリウムとは
過硫酸カリウムとは、硫黄のオキソ酸である過硫酸塩類の1種です。
分子式K₂S₂O₈で表され、分子量は270.32g/molです。別名ペルオキソ二硫酸カリウムと呼ばれています。化学物質固有の番号であるCAS番号は7727-21-1です。
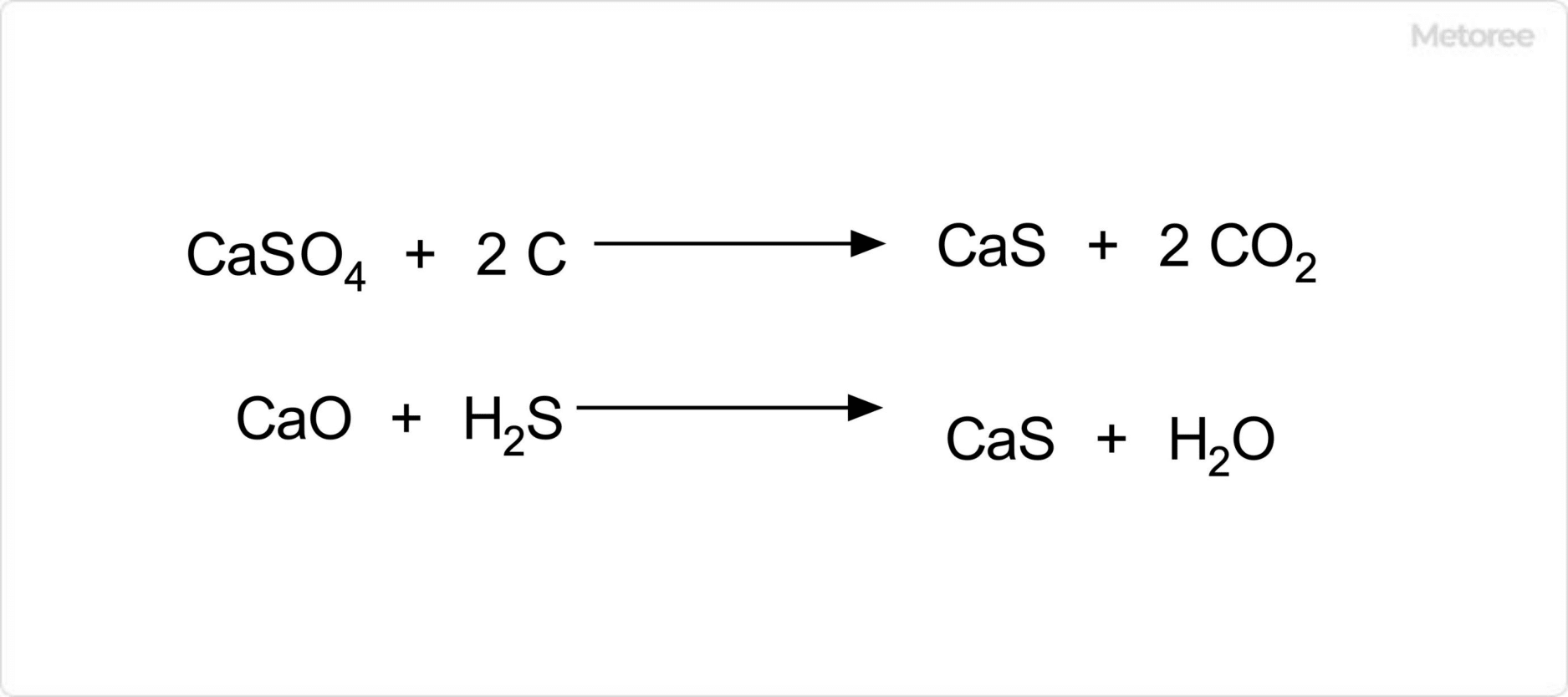
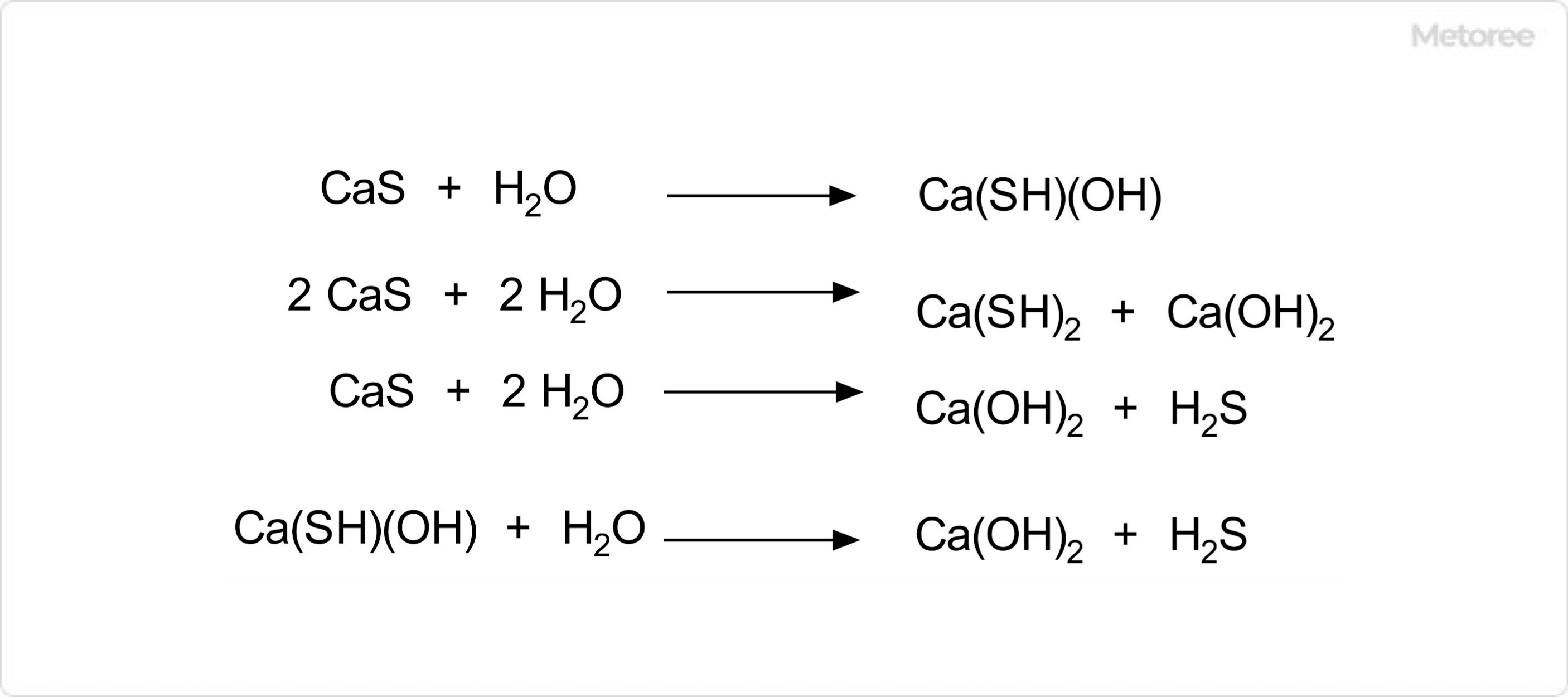
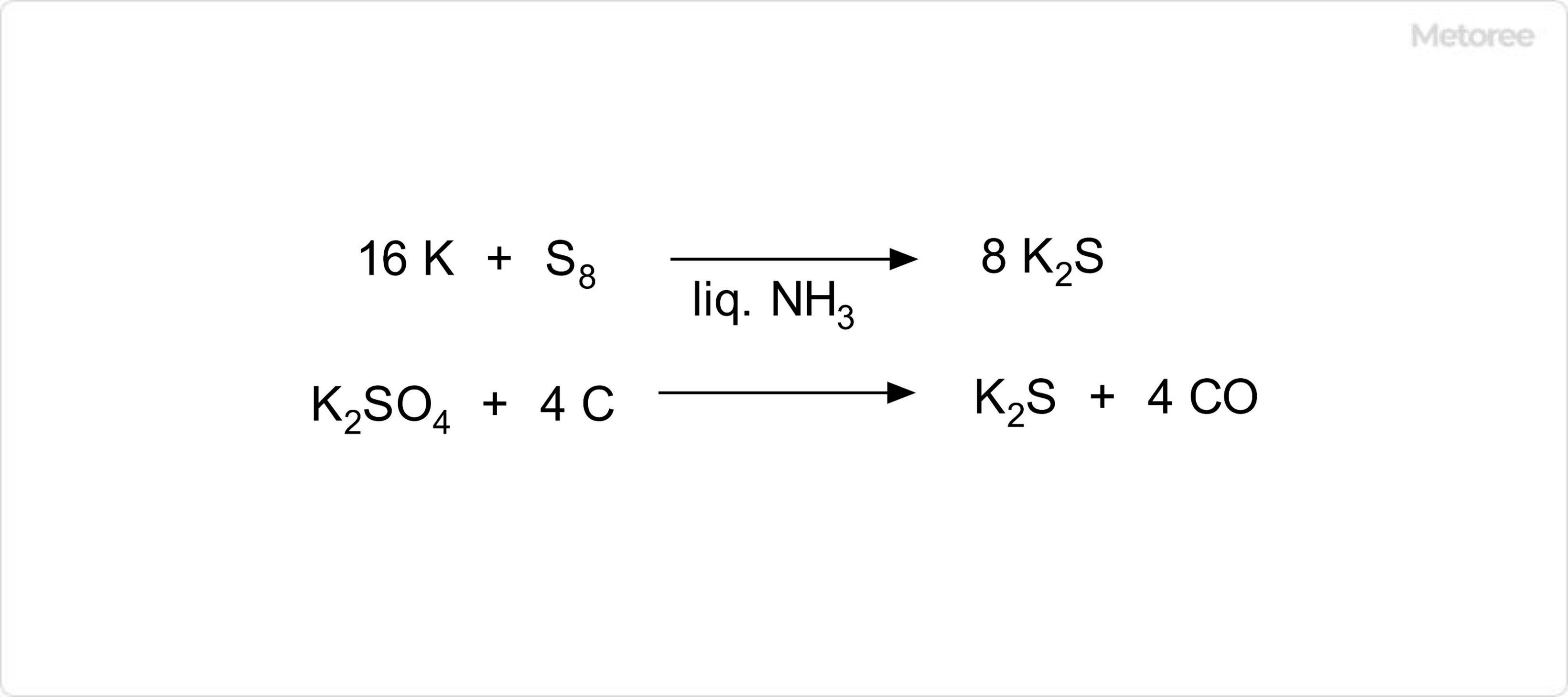
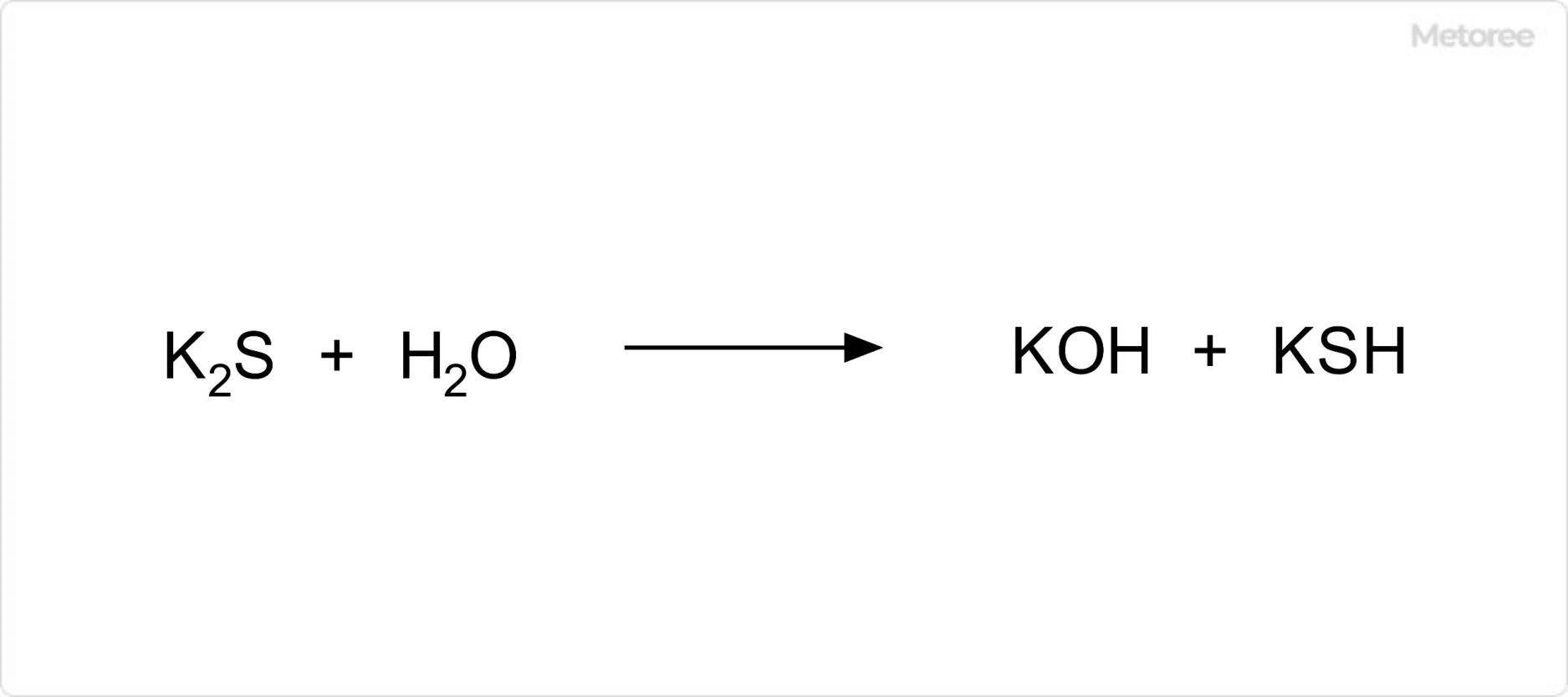
一般的には、過硫酸アンモニウムと水酸化カリウムの水溶液中の反応による製法が知られており、現在でもその方法での製造が行われています。常温常圧では、白色~わずかにうすい黄色を呈した結晶状態として存在しており、無臭です。
水に対する溶解度は20℃で5.2g/100mlと溶けにくいものの、熱水にはよく溶け、エタノールにはほとんど溶けないという性質をもっています。
過硫酸カリウムの使用用途
過硫酸カリウムは、主に以下の用途で使用されています。
- プリントエッチング剤
- 金属の表面処理剤
- デンプン改質剤
- 合成樹脂・合成繊維の重合開始剤
- 土壌改良材
- 天然物の漂白剤
- 医薬品合成酸化剤
プリント基板のエッチング剤は、金属や金属酸化物を腐食させる薬剤であり、主に金属やガラス、半導体などを対象に自身がもつ腐食性を利用して表面を削る表面加工法として用いられます。エッチングは切削や研磨よりも精度の高い加工が一括してできるため、プリント基板の製造だけでなく、半導体の加工やMEMSの加工にも用いられています。
過硫酸カリウムは、強力でありながらも反応がゆっくりと進む酸化剤です。現在でも、フェノールや芳香族アミン、芳香族炭化水素の合成の際の重合開始剤として利用されています。過硫酸カリウムは、工業的に重要な水系重合プロセスである乳化重合の開始剤として働きます。
乳化重合とは、難溶性モノマーを混濁させることで、界面活性剤中に形成された球状ミセルに過硫酸カリウムなどの重合開始剤を加えることで加熱によって重合させる方法です。重合反応する際に生じる発熱の除去や系の粘度を低く抑えられる点で工場での量産化に適しています。
過硫酸カリウムは酸素系の漂白剤に配合されており、天然物の漂白や洗浄などに使用されています。酸素系漂白剤は強塩基であるため、油汚れや皮脂による黄ばみなどに強い性質をもっています。
過硫酸カリウムの性質
過硫酸カリウムは、消防法において第一類酸化性固体に指定されており、自身は燃焼しないが他の物質を強く酸化させる性質をもっています。そのため、可燃物や有機物と混合した際に熱・衝撃・摩擦によって分解し、激しい燃焼を引き起こす強力な酸化剤として働きます。
加熱すると分解し、気体化した二酸化硫黄である亜硫酸ガスが発生します。亜硫酸ガスは無色で刺激臭のある有毒気体であり、還元性があることから、水分がある場合に漂白作用を示すという性質があります。
亜硫酸ガスを吸引した場合には、呼吸器系に強い刺激を与えて喘息を引き起こす場合があるため、注意が必要です。また、強塩基とも激しく反応する性質をもっています。安定性の観点からも光により変質するおそれがあるため、高温、直射日光、熱、静電気から触れるのを防ぐ必要があります。
過硫酸カリウムのその他情報
1. 過硫酸カリウムの法規情報
- 消防法: 第一類酸化性固体 ペルオキソ二硫酸塩類 危険等級Ⅲに該当
- 毒物及び劇物取締法: 非該当
- 化学物質排出管理促進法 (PRTR法) : 第1種指定化学物質に該当
- 船舶安全法及び航空法: 酸化性物質類・酸化性物質に指定
2. 取扱い及び保管上の注意
過硫酸カリウムを取り扱ったり、保管したりする際には、以下の点に注意が必要です。
- 可燃物や還元剤との接触を避ける。
- 周辺で高温物を使用しない。
- 保管場所は壁、柱、床を耐火構造とし、はりを不燃材料で作る。
- 保管場所の屋根を不燃材料で作るとともに、かつ天井を設けない。
- 容器は遮光し、換気がされている涼しい場所に密閉して保管する。
参考文献
https://labchem-wako.fujifilm.com/sds/W01W0116-1189JGHEJP.pdf
https://www.djklab.com/parts/service/pdf/polymer-radical-1.pdf
https://www.adeka.co.jp/chemical/products/commodity/pro162c.html
https://anzeninfo.mhlw.go.jp/anzen/gmsds/0948.html