塩化セシウムとは
塩化セシウムとは、化学式がCsClで表される無機化合物です。
実験室では、水酸化セシウム、炭酸セシウム、重炭酸セシウム、硫化セシウムなどを塩酸で処理すると、塩化セシウムが得られます。
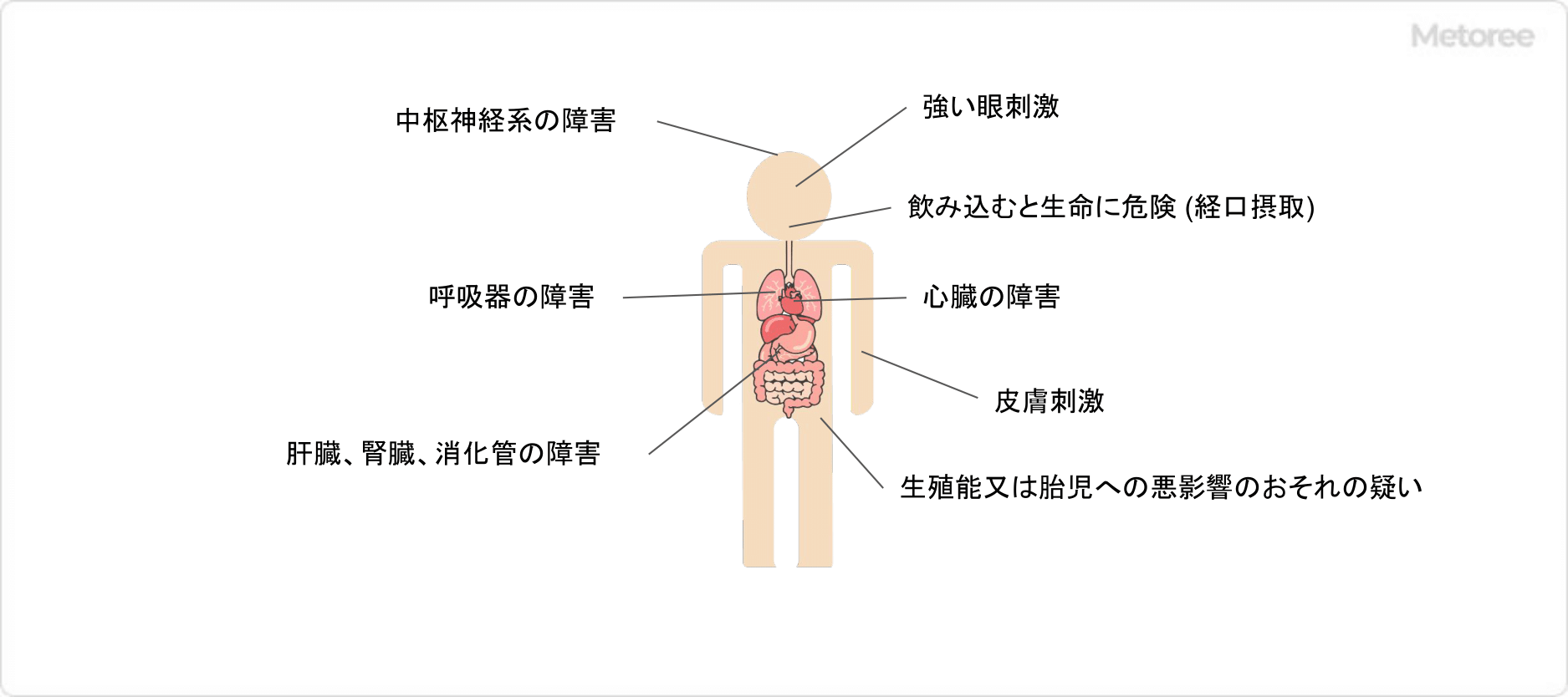
塩化セシウムの人や動物に対する毒性は低いです。GHS分類でいずれも該当していません。労働安全衛生法、労働基準法、PRTR法、毒物・劇物取締法にも非該当です。
塩化セシウムの使用用途
塩化セシウムの使用用途の具体例として、光電管、感光性蒸着膜、蛍光体、触媒、光ファイバー、塩素化剤、密度勾配遠心用試薬などが挙げられます。他のセシウム化合物の合成時に、セシウムイオン源として使用可能です。
とくにDNA分離試薬や真空管材料は、塩化セシウムの特徴的な使用用途です。そのほか放射性同位体としてがん治療のシンチグラフィー (英: scintigraphy) にも用いられています。シンチグラフィーとは、放射性同位体の体内投与による放射線を検出し、画像化する診断法のことです。
塩化セシウムの性質
塩化セシウムの融点は645°Cで、沸点は1,295°Cです。白色の結晶や結晶性粉末です。
塩化セシウムには潮解性があります。水に溶解すると完全に解離して、Cs+が希薄溶液により溶媒和されています。
塩化セシウムを濃硫酸中で加熱するか、硫酸水素セシウムとともに550~700°Cで加熱すると、硫酸セシウムに変換可能です。塩化セシウムは他の塩化物とさまざまな複塩を形成します。具体例として、2CsCl・BaCl2、CsCl・2CuCl、2CsCl・CuCl2、CsCl・LiClなどが挙げられます。
塩化セシウムの構造
塩化セシウムの式量は168.36g/molで、密度は3.99g/cm3です。
固体はイオン結晶で、塩化物イオン (Cl−) とセシウムイオン (Cs+) から構成される単純立方格子です。それぞれの塩化物イオンはセシウムイオン8つと隣接しています。1:1の組成比を有する塩の結晶で、2種類のイオンの半径がほぼ等しい場合には塩化セシウム型の構造を取ります。塩化セシウム型構造は、イオン結晶の代表的な構造の一つです。塩化セシウム型構造を形成する化合物は、ヨウ化セシウムや臭化セシウム以外にも、銅と亜鉛や鉄とロジウムの1:1合金が知られています。
塩化セシウムの格子定数はa = 0.411nmで、原子間距離Cs-Clは0.345nmです。450°C以上では岩塩型構造に転移します。
塩化セシウムのその他情報
1. 天然の塩化セシウム
天然にはハロゲン化鉱物であるカーナライト (最大0.002%のCsClを含むKMgCl3・6H2O) 、カリ岩塩 (KCl)、カイナイト (MgSO4・KCl・3H2O) 、ミネラルウォーターなどに、不純物として塩化セシウムは存在します。例えば、セシウムの分離に使用されたバート・デュルクハイムのスパの水中には、約0.17mg/Lの塩化セシウムが含まれていました。
2. 塩化セシウムの合成法
工業的には炭酸セシウムを塩酸に溶解し、再結晶して塩化セシウムを精製可能です。塩化セシウムはポルックス石 (英: Pollucite) から生産され、抽出物を塩化アンチモン、一塩化ヨウ素、塩化セリウム(IV)で処理すると、難溶性複塩として生成します。硫化水素によって、塩化セシウムが得られます。熱分解したCs[ICl2]やCs[ICl4]を再結晶すると、高純度の塩化セシウムを生成可能です。
3. 塩化セシウムの危険性
マウスによる塩化セシウムの致死量の中央値 (LD50) は、経口投与で体重1kgあたり2,300mgで、静脈内注射で910mg/kgです。塩化セシウムはカリウムを部分的に置換するため、体内のカリウム濃度が低下します。塩化セシウムを大量に摂取すると、カリウムのバランスが崩れて、低カリウム血症、不整脈、急性心停止を引き起こす可能性があります。
参考文献
https://labchem-wako.fujifilm.com/sds/W01W0103-0195JGHEJP.pdf