次亜硫酸ナトリウムとは
次亜硫酸ナトリウムとは、亜ジチオン酸のナトリウム塩です。
他にも「亜ジチオン酸ナトリウム」「亜二チオン酸ナトリウム」「ハイドロサルファイトナトリウム」と呼ばれています。単にジチオナイトと呼ぶ場合には、次亜硫酸ナトリウムや溶解して得られる亜ジチオン酸イオンを指すケースが多いです。
次亜硫酸ナトリウムの粉末が、空気中で少量の水と接すると、分解で生じる熱により、引火することもあります。労働安全衛生法では、名称等を表示すべき危険物および有害物に該当します。
次亜硫酸ナトリウムの使用用途
次亜硫酸ナトリウムは亜硫酸ナトリウムと同様に、食品添加物として食品加工で使用されることが多いです。最も多い利用は、ワインなどの飲料における酸化防止剤です。
また、水に溶けやすく、強力な還元作用を持つことから、漂白剤や変色防止剤として使用されることもあります。食品の色調を整えたり、原料などに含まれる好ましくない色素成分や着色物質の色を無色にしたりすることも可能です。
世界における次亜硫酸ナトリウムのうち、半分が織物の染色や漂白に、3分の1がパルプや紙の漂白などに使用されています。なお、次亜硫酸ナトリウムは、工業的には金属亜鉛を仲介した二酸化硫黄とナトリウム塩の反応によって精製されます。
次亜硫酸ナトリウムの性質
次亜硫酸ナトリウムは、常温では白色結晶です。亜硫酸ガスと同様の刺激臭がします。引火点は100°C、発火点は200°Cです。
次亜硫酸ナトリウムはエタノールにわずかに溶け、水に溶けやすいです。融点は52°Cで、空気中で90℃以上に加熱することで、硫酸ナトリウムと二酸化硫黄に分解されます。空気がない場合には、150℃以上で亜硫酸ナトリウム、チオ硫酸ナトリウム、二酸化硫黄、微量の硫黄に激しく分解されます。
次亜硫酸ナトリウムの構造
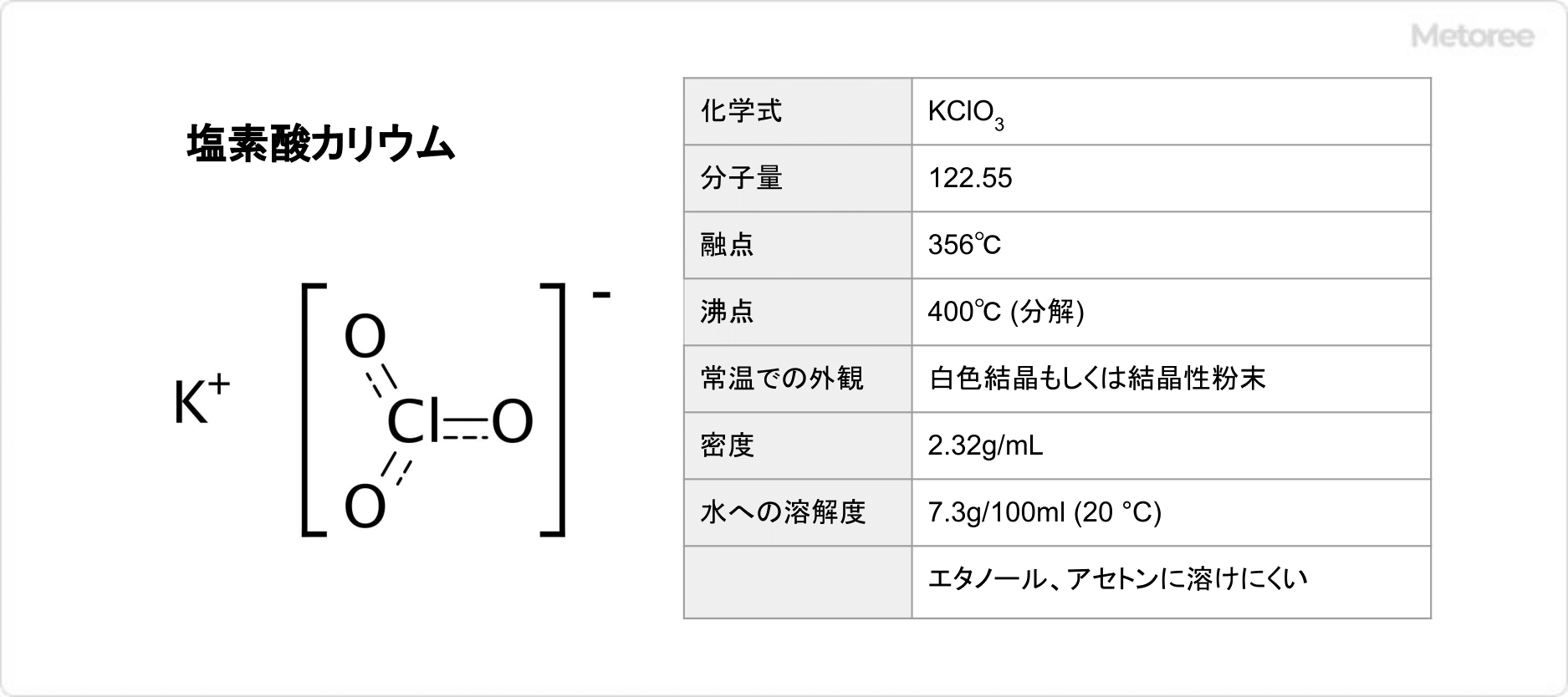
次亜硫酸ナトリウムの化学式はNa2S2O4、モル質量は174.107、密度は2.19g/cm3です。次亜硫酸ナトリウムの無水物は、白色の単斜晶です。二水和物も知られており、黄色味がかった柱状結晶ですが、容易に脱水して無水物になります。さらに二水和物は空気中の酸素によって酸化されやすいため、不安定です。
次亜硫酸ナトリウムの無水物は、C2対称構造を取り、ねじれ角16°の重なり形配座です。その一方で二水和物は、ねじれ角56°のゴーシュ配座になっています。
次亜硫酸ナトリウムのその他情報
次亜硫酸ナトリウムの合成方法
1. 亜鉛塵法による合成
亜鉛の粉末を水に懸濁させ、二酸化硫黄を通すことで、亜鉛が溶け、亜ジチオン酸亜鉛になります。炭酸ナトリウムや水酸化ナトリウムを加えることで、水酸化亜鉛 (II) の白色沈澱として亜鉛を析出させて、減圧濃縮後に塩化ナトリウムとメタノールを加えると、次亜硫酸ナトリウムの無水物が析出します。
2. ギ酸ソーダ法による合成
ギ酸ソーダ法は三菱ガス化学が実用化した方法です。ギ酸ナトリウムを80%のメタノールに溶かして、水酸化ナトリウムと二酸化硫黄を加えると、次亜硫酸ナトリウムの無水物が析出します。多価アルコールを製造する際に副生成物としてギ酸ナトリウムが得られるため、亜鉛塵法よりも低コストなことが利点です。
3. アマルガム法による合成
食塩電解槽で作成したナトリウムアマルガムを、亜硫酸水素ナトリウム水溶液に接触させて、還元することにより次亜硫酸ナトリウムが得られます。
4. 水素化ホウ素ナトリウム法による合成
強アルカリ水溶液中において安定な還元剤である水素化ホウ素ナトリウムに、二酸化硫黄と水酸化ナトリウムを加えることで、次亜硫酸ナトリウムが生成します。
5. 電解法による合成
半透膜で仕切られた電解槽を用いて、二亜硫酸イオンを還元すると、次亜硫酸ナトリウムが生じます。