アセト酢酸エチルとは
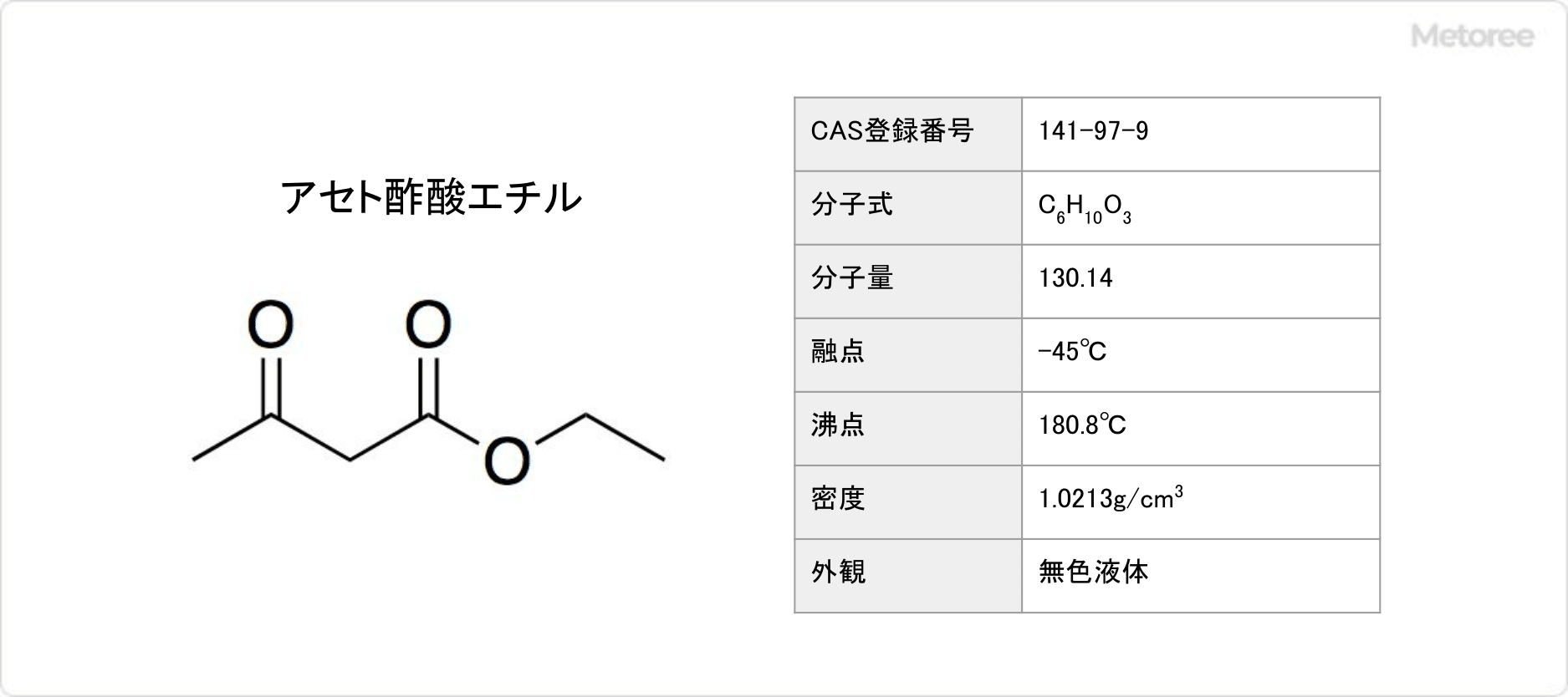
アセト酢酸エチル (英: Ethyl acetoacetate) とは、化学式がC6H10O3で表される、アセト酢酸のエチルエステルです。
3-オキソブタン酸エチル (英: Ethyl 3-oxobutanoate) とも呼ばれています。果実のような特徴的な臭気があり、無色の可燃性液体です。消防法の危険物第4類、第3石油類非水溶性液体に分類されます。
アセト酢酸エチルに塩基を作用させて生じる比較的安定なカルバニオンは、炭素-炭素結合の生成反応によく利用されます。
アセト酢酸エチルの使用用途
アセト酢酸エチルは他のエステルよりも反応性が高いため、種々の有機合成原料に使用されます。具体例を挙げると、解熱鎮痛剤、抗マラリア剤、抗生物質、アミノ酸、ビタミンBなどの化合物の製造で、中間体として利用可能です。
また、フルーティーな臭気を持つため、食品のフレーバー(着香剤)や香水等としても用いられます。その他、ラッカー塗料、染料製造、プラスチック製造、分析試薬としても使用可能です。
アセト酢酸エチルの性質
アセト酢酸エチルの融点は−45°Cで、沸点は180.8°Cであり、引火点は70°Cで、20°Cで屈折率は1.41937です。20°Cで100mLの水に2.86g溶けます。エタノールやアセトンに極めて溶解しやすいです。
アセト酢酸エチルの2位のメチレン部位上の水素原子は、比較的高い酸性を示します。25°CでのpKaは10.7です。
アセト酢酸エチルを希酸や希アルカリによって加水分解すると、二酸化炭素が生じて、アセトンが生成します。ただし強アルカリと反応すると酢酸になります。
アセト酢酸エチルの構造
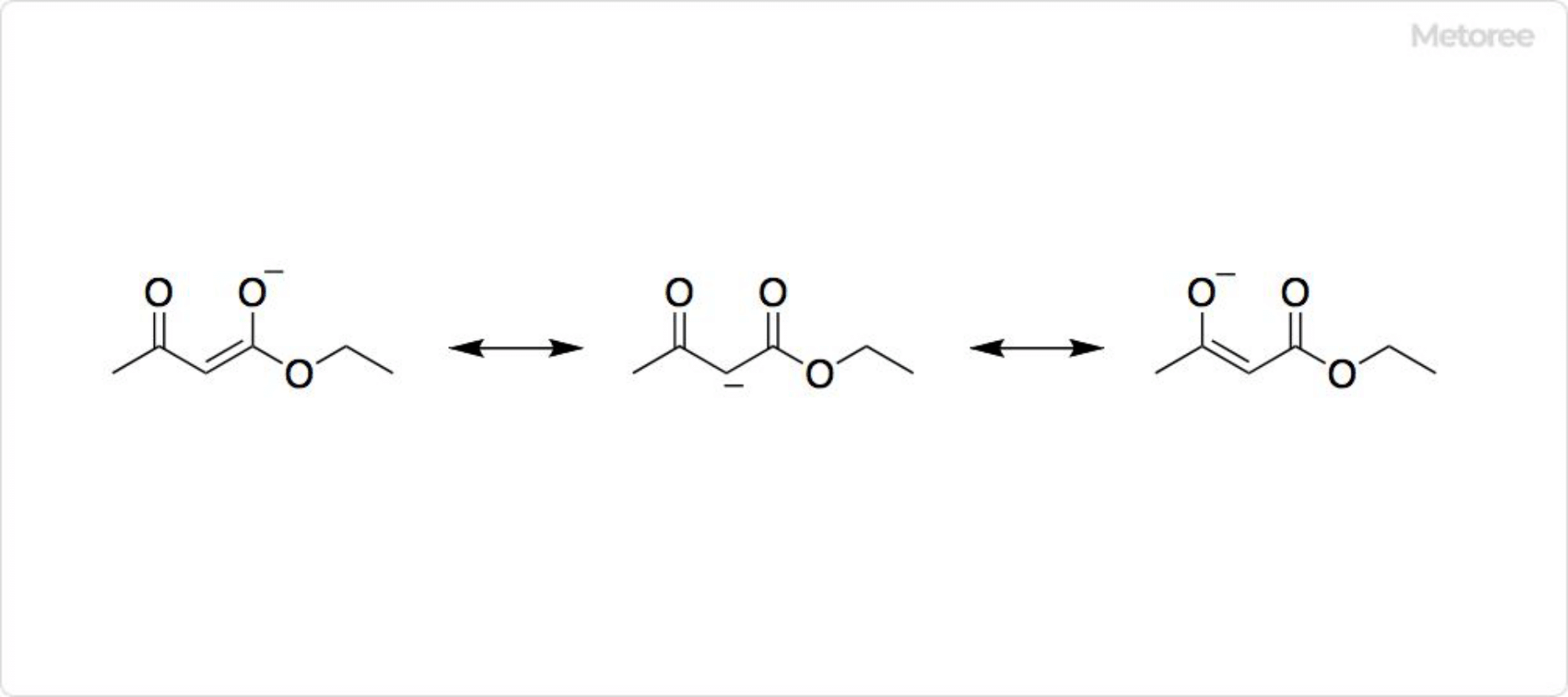
図2. アセト酢酸エチルの構造
アセト酢酸エチルの示性式は、CH3COCH2COOC2H5で表されます。分子量は130.14g/molで、25°Cでの密度は1.021g/cm3です。
アセト酢酸エチルはケトエノール互変異性 (英: keto-enol tautomerism) の影響を受けます。33°Cでエノールは、全体の15%です。
アセト酢酸エチルの共役塩基であるカルバニオンも、2種類のエノラート構造と共鳴の関係にあります。したがって負電荷が非局在化しており、安定化されています。
アセト酢酸エチルのその他情報
1. アセト酢酸エチルの合成法
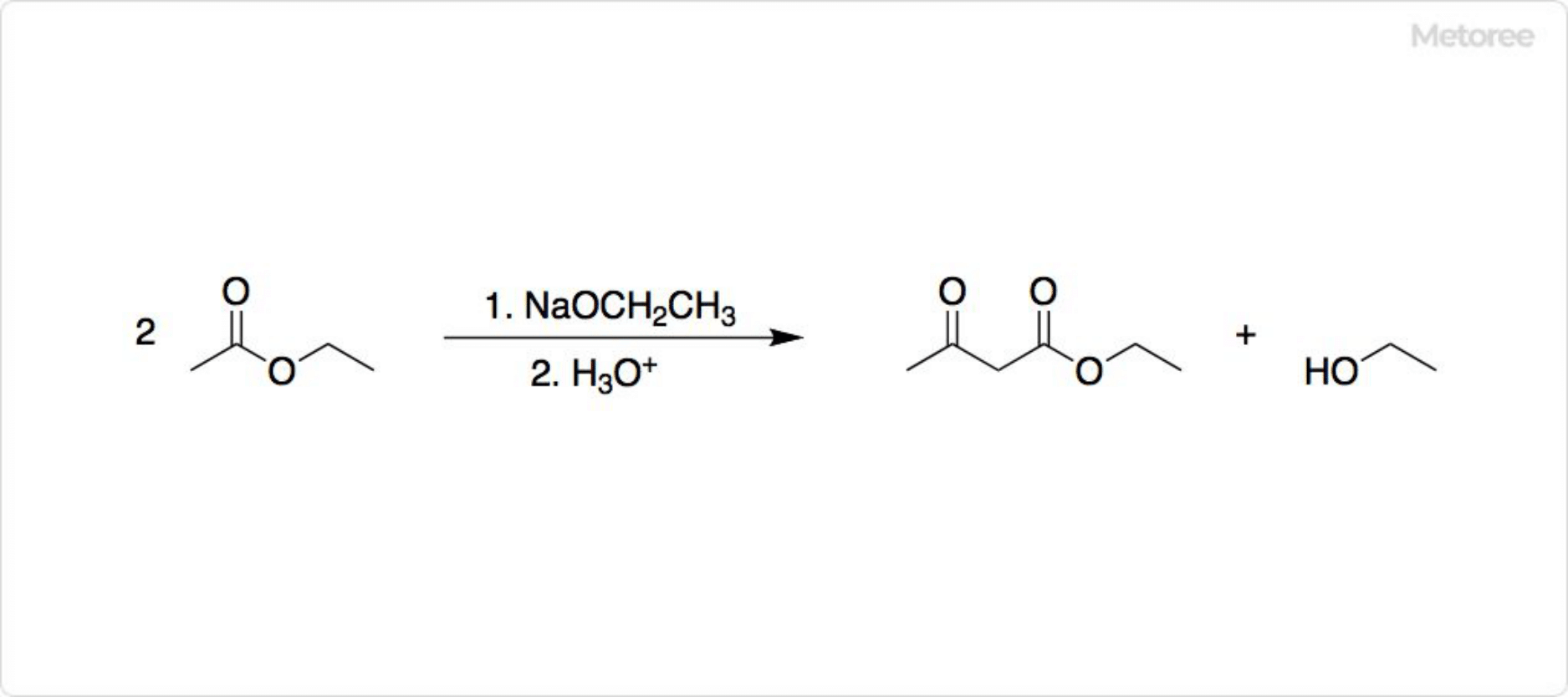
図3. アセト酢酸エチルの合成
酢酸エチルに金属ナトリウムなどを反応させると、アセト酢酸エチルが得られます。酢酸エチルにナトリウムエトキシドを加えて、縮合させても合成できます。ナトリウムエトキシドの化学式はC2H5ONaです。これらの反応はクライゼン縮合 (英: Claisen condensation) と呼ばれます。
工業的には、ジケテンをエタノールで処理して、アセト酢酸エチルが製造されます。
2. アセト酢酸エチルの反応
アセト酢酸エチルは活性メチレンを有し、塩基によって比較的安定なカルバニオンが生成します。活性メチレン (英: activated methylene) とは、カルボニル基のような電子求引基2つに挟まれたメチレン基のことです。
活性メチレンの影響で酸性が強い化合物には、マロン酸エステル、シアノ酢酸エステル、アセチルアセトンなどがあります。カルバニオンの安定性は、炭素-炭素結合形成のために利用可能です。具体例として、アセト酢酸エステル合成 (英: acetoacetic ester synthesis) やマロン酸エステル合成 (英: malonic ester synthesis) が挙げられます。
アセト酢酸エチルなどの活性メチレン化合物は、クロスカップリング反応 (英: Coupling reaction) やマイケル付加反応 (英: Michael addition) でも使用されます。