硝酸ニッケルとは
硝酸ニッケル (英: Nickel Nitrate) とは、組成式Ni(NO3)2で表されるニッケルの硝酸塩です。
無水物のCAS登録番号は13138-45-9ですが、通常は水和物を指します。最も多い六水和物Ni(NO3)2・6H2OのCAS登録番号は、13478-00-7です。
火災を助長する可能性のある物質であるほか、眼や皮膚に対する刺激性があり、皮膚への接触や吸入によりアレルギー反応を示し、発癌のおそれがあります。
硝酸ニッケルの使用用途
硝酸ニッケルの主な用途は、アルカリ蓄電池やニッケル・水素充電池、触媒、金属表面処理剤、セラミック用顔料原料などです。
1. 二次電池
ニッケルカドミウム電池、ニッケル水素電池など、携帯電話やデジタルカメラに使用されている充電式電池です。硝酸ニッケルは、添加剤として多く使用されています。
2. 触媒
合成樹脂や合成繊維の重合触媒として使われている物質です。
3. 表面処理
家電、自動車用の鋼板、プリント基板用銅箔など、メッキ薬品や表面処理薬品原料として利用されています。
4. 着色
樹脂やアルミ、ガラスの着色剤、発色剤として使われている物質です。
それ以外では、他のニッケル誘導体の水配位子交換の前駆物質として水和物が用いられることがあります。
硝酸ニッケルの性質
1. 硝酸ニッケル (無水物) の基本情報
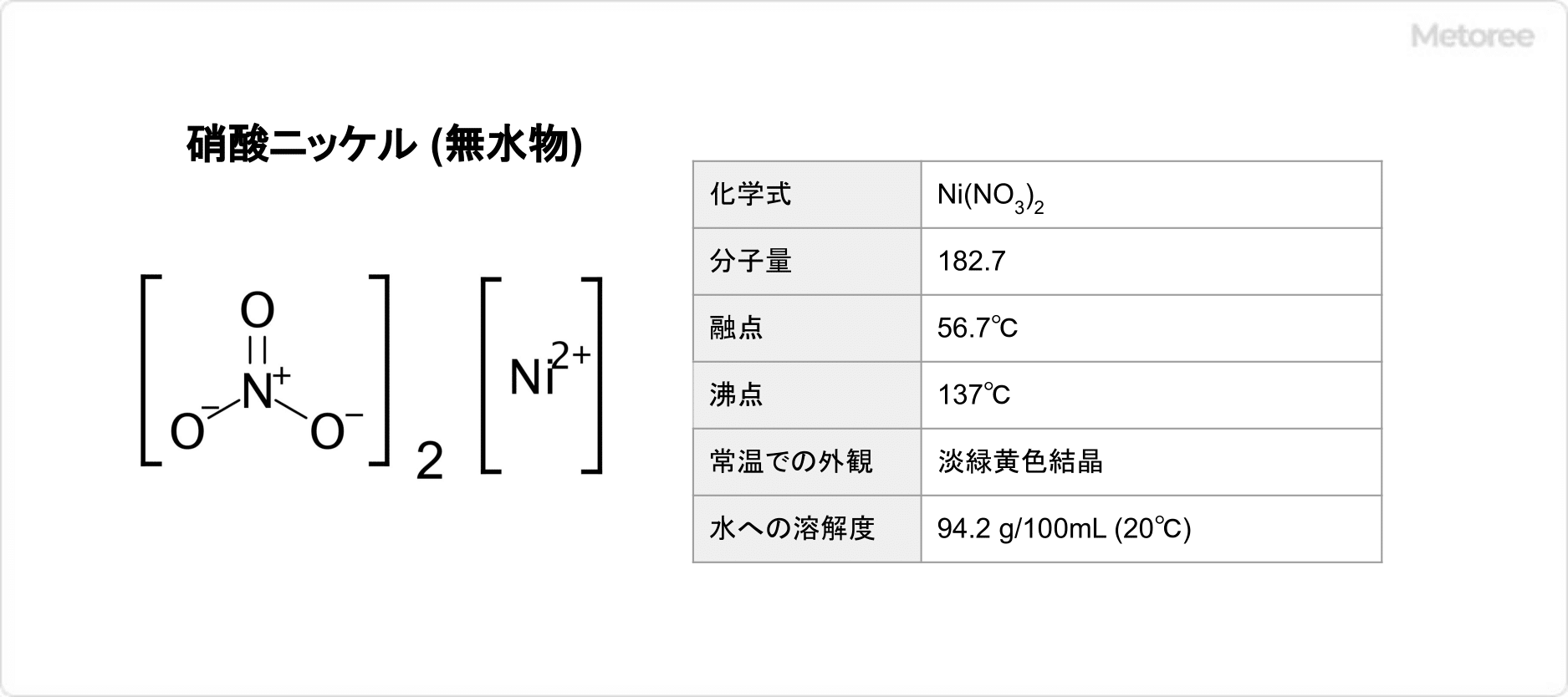
図1. 硝酸ニッケル(無水物)の基本情報
硝酸ニッケルの無水物は、分子量182.7、融点56.7℃、沸点137℃であり、常温での外観は淡緑黄色結晶です。水への溶解度は 94.2g/100ml (20℃) です。潮解性があります。水溶液は緑色です。
2. 硝酸ニッケル (六水和物) の基本情報
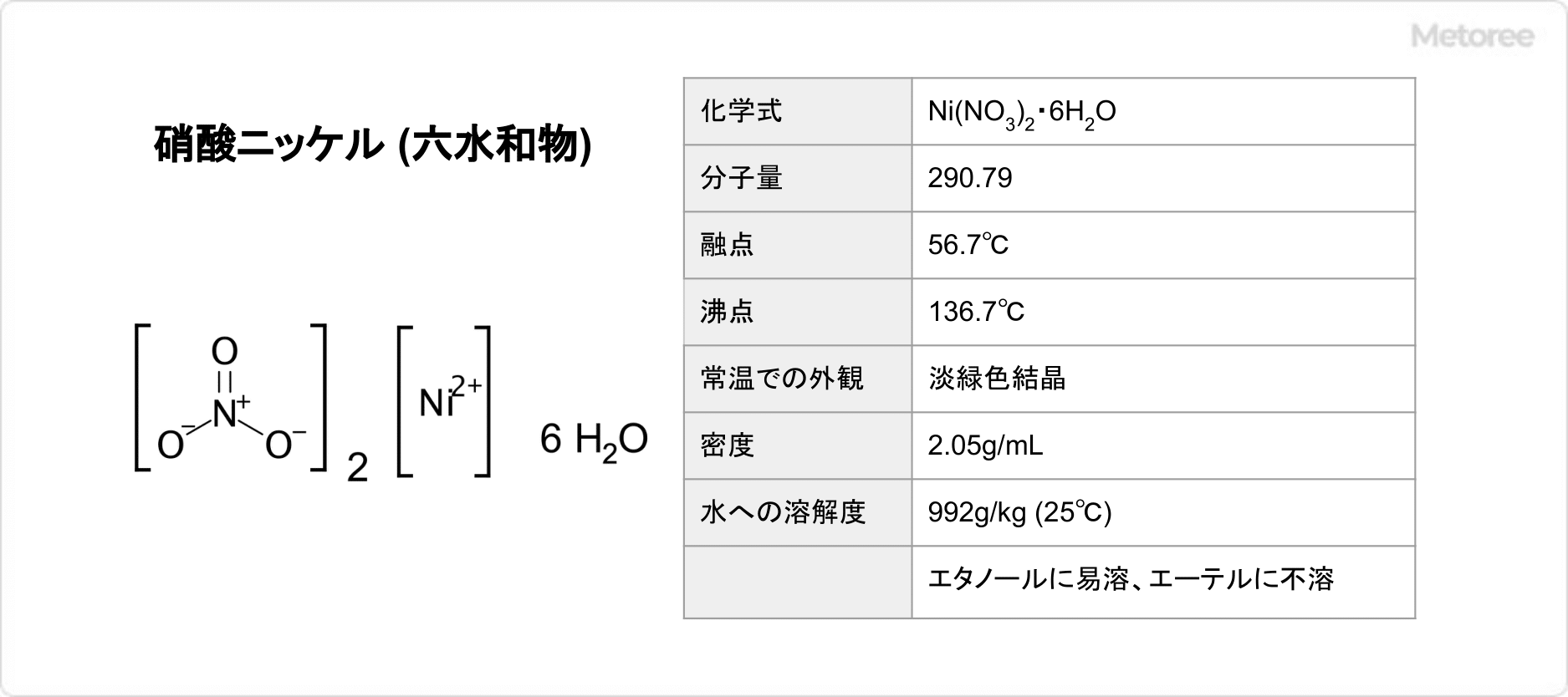
図2. 硝酸ニッケル(六水和物)の基本情報
硝酸ニッケル六水和物は、分子量290.79、融点56.7℃、沸点136.7℃であり、常温での外観は淡緑色結晶です。湿気の多い場合は潮解性、少ない場合は風解性を示します。密度は2.05g/mLであり、水に溶解しやすく、水への溶解度は992g/kg (25℃) です。また、エタノールに溶けやすく、エーテルに不溶です。
結晶は単斜晶系に属します。加熱によってまず結晶水を部分的に失って二水和物となり、更に硝酸を失い、塩基性塩を経て酸化ニッケルになります。
硝酸ニッケルの種類
硝酸ニッケルは、主に研究開発用試薬製品や工業用無機金属化合物として販売されています。基本的には六水和物の状態で販売されることが一般的です。
1. 研究開発用試薬製品
研究開発用試薬製品としては、20g、100g、500gなどの単位で販売されています。通常、室温で保管可能な試薬製品として販売されている物質です。ただし、潮解性があるため、取り扱いに注意が必要です。
2. 工業用無機金属化合物
工業用無機金属化合物としては、20kgポリ袋などの単位で販売されていることが一般的です。金属表面処理剤、めっき、触媒、二次電池正極材、など様々な用途が想定されており、複数のメーカーから販売されています。
硝酸ニッケルのその他情報
1. 硝酸ニッケルの合成
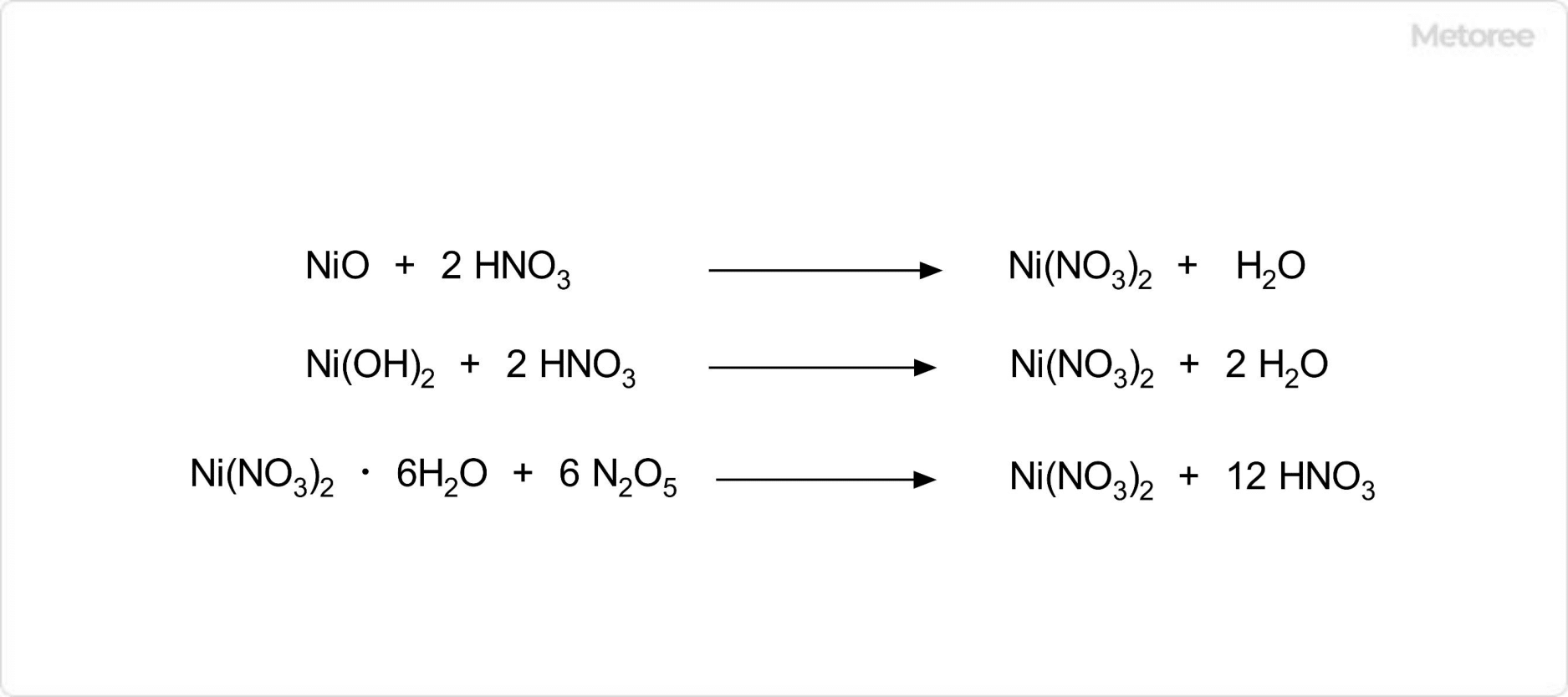
図3. 硝酸ニッケルの合成
硝酸ニッケルは、酸化ニッケル、または水酸化ニッケルと希硝酸を反応させることで、合成が可能です。本反応では、濃縮することで、六水和物が得られます。多くは、この六水和物を硝酸ニッケルとして販売、使用されています。
無水物は六水和物に純硝酸と五酸化二窒素の混合物を作用させることによって、合成が可能です。
2. 硝酸ニッケルの反応性
硝酸ニッケルは通常の保管環境においては安定な物質ですが、酸化性を持ち、可燃物やマグネシウム、硫黄などと激しく反応します。不燃性の物質ですが、火災等の場合は、毒性の強い分解生成物が発生する可能性があります。
参考文献
https://anzeninfo.mhlw.go.jp/anzen/gmsds/13138-45-9.html
https://anzeninfo.mhlw.go.jp/anzen/gmsds/13478-00-7.html