システインとは
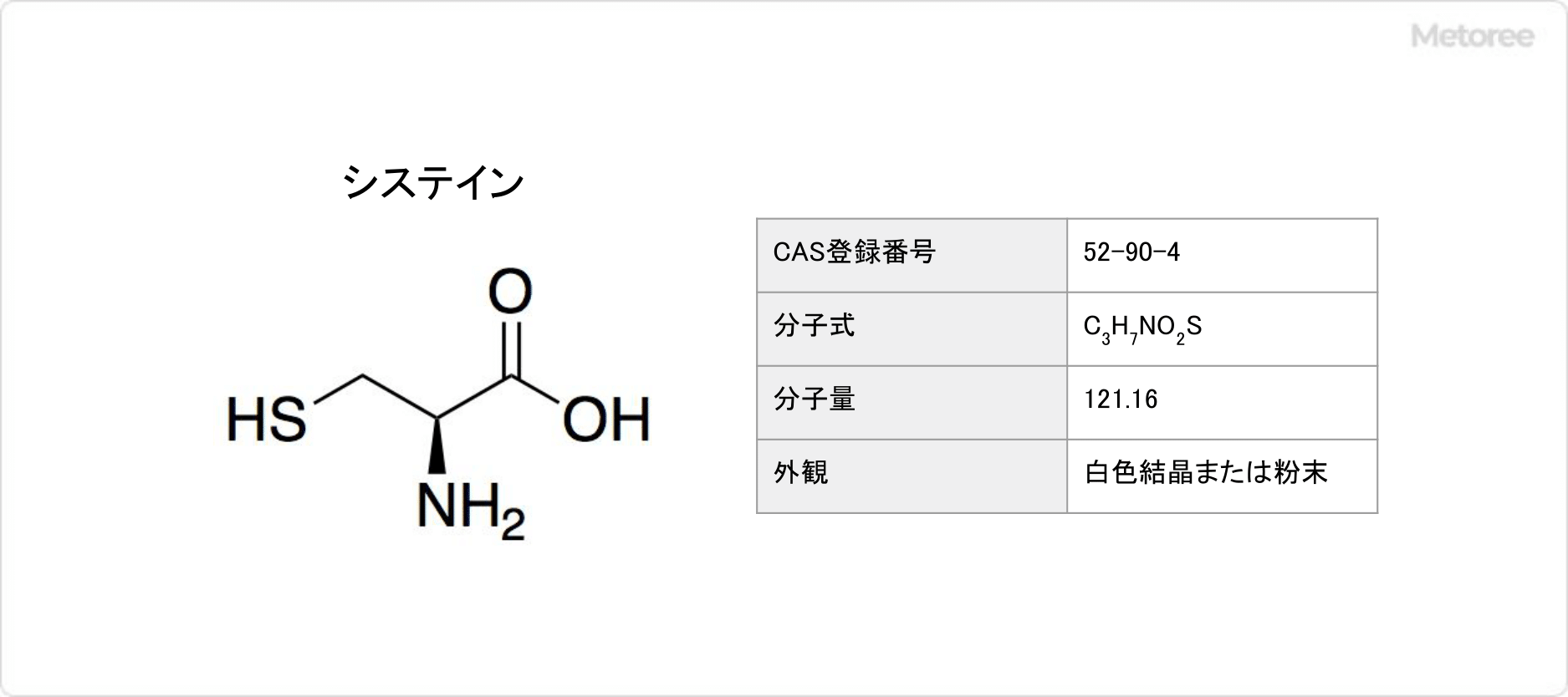
システインとは、側鎖にチオール基を有する非必須アミノ酸の1つです。
略号はCysで、天然に存在するのはL-システインのみです。皮膚の色素沈着をもたらす原因である黒いメラニン色素の生成を抑え、体外への排出を促進する働きがあります。
また、L-システインはタンパク質の構成物質で、二日酔いの主な原因とされるアセトアルデヒドと直接反応し、毒性を中和可能です。二日酔い改善の効果があるため、健康食品などに利用されています。
システインの使用用途
システインのL体であるL-システインは、医薬品や食品添加物などに使用可能です。 L-システインには、体内で坑酸化作用や肝臓の解毒作用があります。
これらの特性から、抗アレルギー薬、皮膚疾患、放射線などによる白血球減少を抑制する医薬品等に用いられています。さらに、しみ、そばかす、日焼けなどの対策としてビタミンCなどの成分とともに、美白・美容のサプリメント等に有用です。
その他、二日酔い薬としても広く利用されています。
システインの性質
システインは、タンパク質を構成するアミノ酸の1つであり、糖原性を有します。比旋光度[α]Dは+9.4°で、240°Cで分解します。
システイン持つチオール基は、求核性触媒として働き、非常に反応性が高いです。チオール基のpKaはおよそ8で、反応性は環境や条件により変化します。
システインの構造
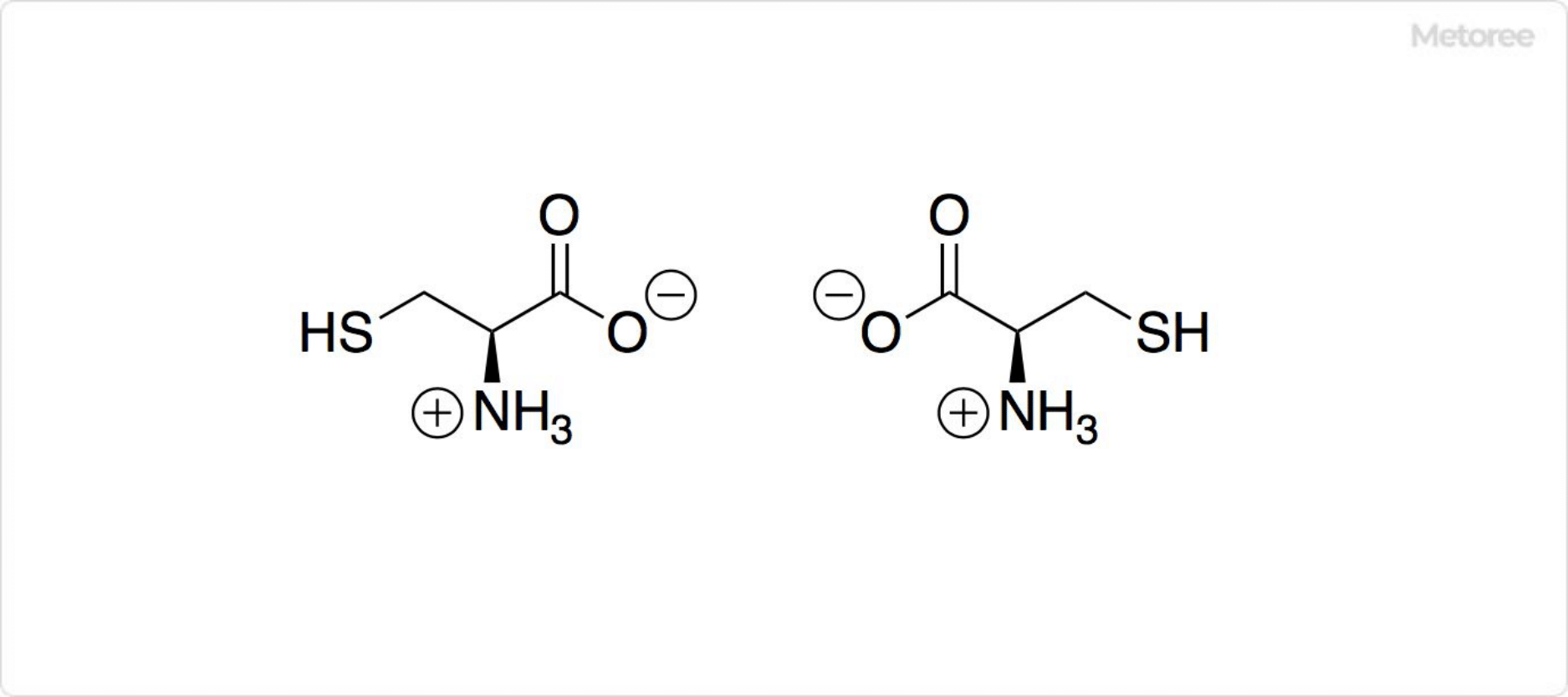
図2. システインの構造
システインは、2-アミノ-3-スルファニルプロピオン酸を指します。分類上は、疎水性アミノ酸や中性極性側鎖アミノ酸です。
多くのアミノ酸と同じく、中性では両性イオンになっています。システインは不斉炭素原子を持っているため、R-システインとS-システインが存在します。R-システインはL-システイン、S-システインはD-システインのことです。
順位則の関係上、他のアミノ酸とは異なり、L-システインのみがR配置となります。なお、システインの化学式はC3H7NO2S、モル質量は121.16g/molです。
システインのその他情報
1. システインの生合成
動物による生合成でシステインの原料になるのは、アミノ酸のセリンです。まず、メチオニンが中間体のS-アデノシルメチオニンを経由して、ホモシステインに変換されます。
次に、シスタチオニンβ合成酵素によって、ホモシステインとセリンが結合して、非対称チオエーテルシスタチオニンが生じます。そして、シスタチオニンγ-リアーゼによって、α-ケト酪酸とともにシステインを生成可能です。
植物や細菌による生合成の場合にも、セリンから作られます。セリントランスアセチラーゼにより、O-アセチルセリンに変換され、システインシンターゼによりO-アセチルセリンからアセテートが脱離し、スルフィド源によりシステインが生成可能です。
2. システインの酸化

図3. システインのジスルフィド結合
システインは酸性条件下では安定ですが、中性やアルカリ性では、微量の重金属イオンによって空気酸化されやすく、シスチンが生成します。シスチンとは3,3’-ジチオビス (2-アミノプロピオン酸) のことで、システインの2つの分子が、チオール基 (–SH) の酸化で生じるジスルフィド結合 (S–S) で繋がった構造を有します。
天然に多く存在するシスチンは、L体 (R,R’体) です。酸化型のシスチンと区別するために、還元型を強調して、システインをCySHと表記する場合もあります。システインがシスチンに酸化されると、求核剤としての能力を失います。
3. システインの生化学
システインの持つチオール基は、分子間でタンパク質を架橋します。システイン同士のジスルフィド結合は、タンパク質ジスルフィド異性化酵素により生成可能です。細胞内では、デヒドロアスコルビン酸が小胞体に輸送されて、酸化的な環境が生じます。
システイン同士のジスルフィド結合によって、分子の安定性が細胞外でも増して、タンパク質が分解しないための抵抗性が向上します。タンパク質の三次構造も、細胞内でポリペプチドに含まれているシステイン間のジスルフィド結合により維持可能です。
例えばインスリンは、システインにより架橋されたペプチドです。独立した2個のペプチド鎖が、1組のジスルフィド結合で繋がっています。システインのジスルフィド結合の配列によって、毛髪の巻き毛の度合いが決定されます。