フルフラールとは
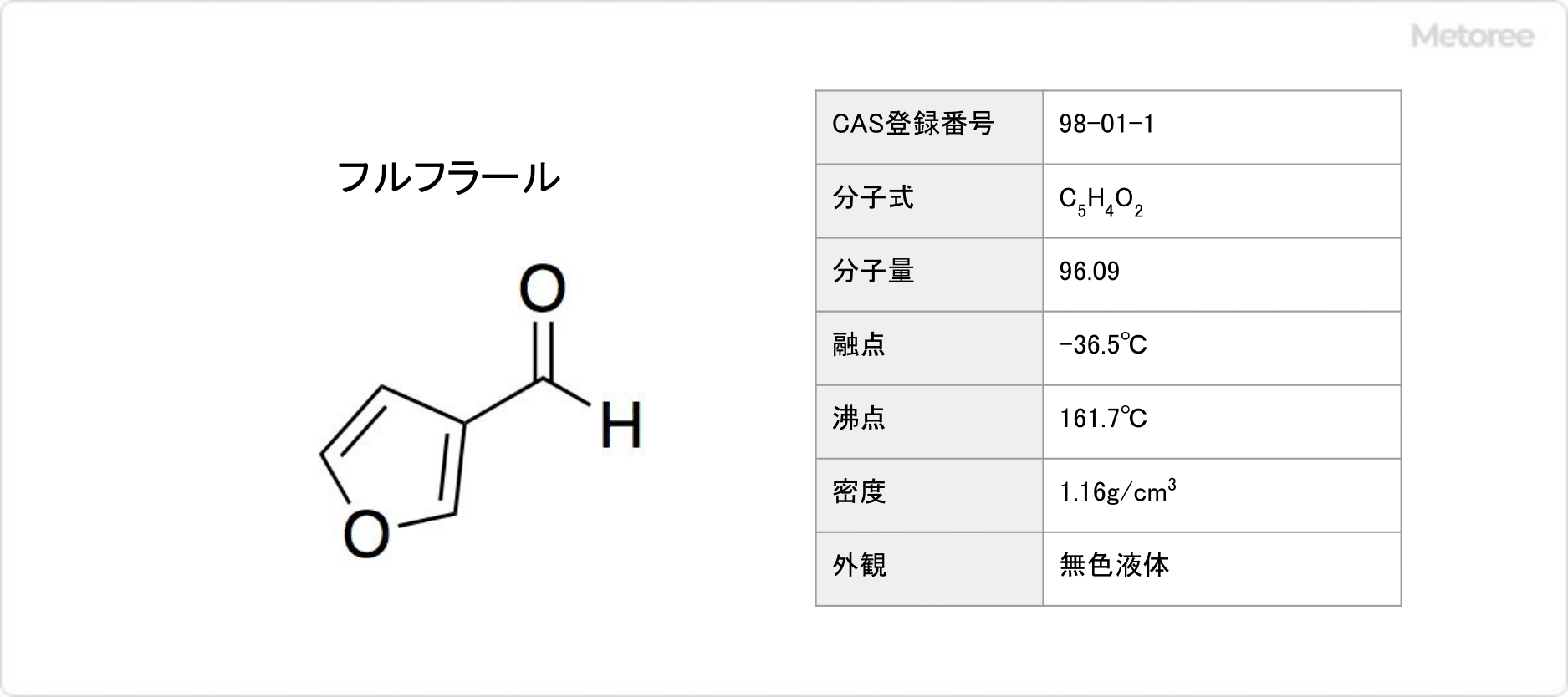
フルフラールとは、化学式がC5H4O2で表される、芳香族アルデヒドの1種です。
2-フランカルボキシアルデヒドとも呼ばれます。1832年にヨハン・オルフガング・デーベライナー (英: Johann Döbereiner) によって、初めてギ酸の副産物として分離されました。
工業的には、トウモロコシの芯やサトウキビのバガスなどの農業副産物から、世界中で数十万トンが生産されています。原料を高圧蒸気下で処理した後、蒸留によって回収し、水とフルフラールを分離可能です。バイオマス由来の安価で再生可能な非石油ベースの化学原料として注目されています。
フルフラールの使用用途
フルフラールは、熱硬化性、耐食性、物理的耐性などの優れた特性を備えており、樹脂の原料として利用されます。例えば、耐薬・耐熱性表面処理剤として用いられているフラン樹脂が挙げられます。
また、フルフラールは、アルコール、エステル、アセトンなどの有機溶剤に混ざるため、溶剤として広く利用されています。主に潤滑油や脱色剤の精製に使用可能です。その他、除草剤や殺虫剤としても利用されます。
フルフラールの性質
フルフラールの融点は-36.5°C、沸点は161.7°Cであり、引火点は62°Cです。無色油状の液体ですが、空気に触れるとすぐ黄色く変色します。
フルフラールはアーモンドに似た香気を有します。エーテルやアルコールなどの、多くの有機溶剤に溶けますが、アルカン類や水には微溶です。
一般的な芳香族化合物やアルデヒド類と同様の化学反応を起こします。ただし、ベンゼンほど安定しておらず、ほかの芳香族化合物と比べて化学反応を起こしやすいです。
例えば、フルフラールを250°C以上に熱すると、一酸化炭素とフランに分解します。酸とともに加熱すると、熱硬化性樹脂になり固まります。強い酸や塩基との反応によって、火災や爆発の危険性もあるため、取り扱いには注意が必要です。
フルフラールの構造
フルフラールは、フランの2位がホルミル基で置換された構造を有します。示性式は(C4H3O)CHOで表され、モル質量は96.09g/mol、密度は1.16g/mLです。
フルフラールのその他情報
1. フルフラールの合成
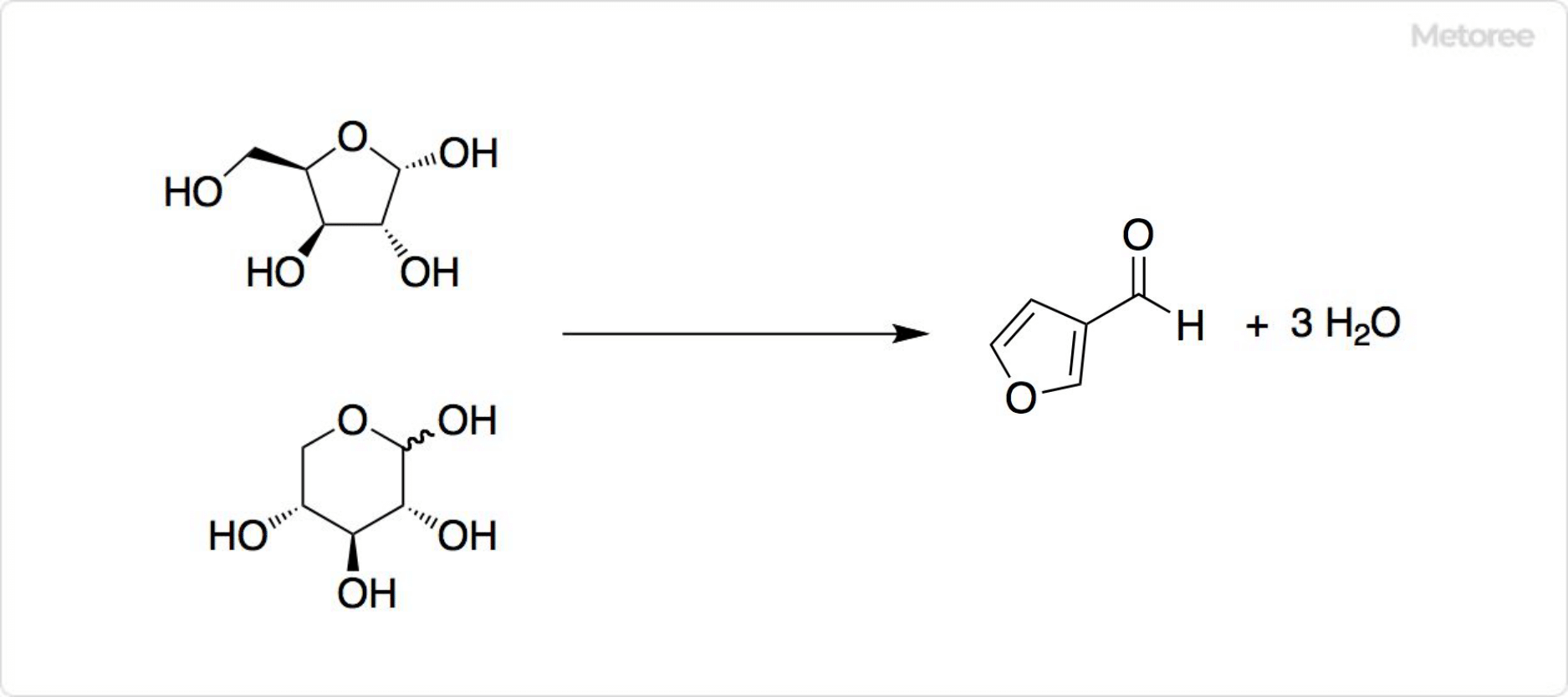
図2. フルフラールの合成
多くの植物には、多糖類やヘミセルロースが含まれています。そのため、希硫酸とともに熱すると、ヘミセルロースの加水分解によって、キシロースのような糖類に変化します。同条件下でキシロースなどのC5糖類の脱水によって、3個の水分子を放出し、フルフラールを生成可能です。希硫酸の代わりに希塩酸を使用する方法もあります。
トウモロコシや燕麦殻の場合には、収率は比較的高く、20%ほどです。穀物の籾殻を用いると、原料のおよそ10%のフルフラールが得られます。水とともにフルフラールが蒸発するため、分離回収して濃縮できます。
2. 原料としてのフルフラール
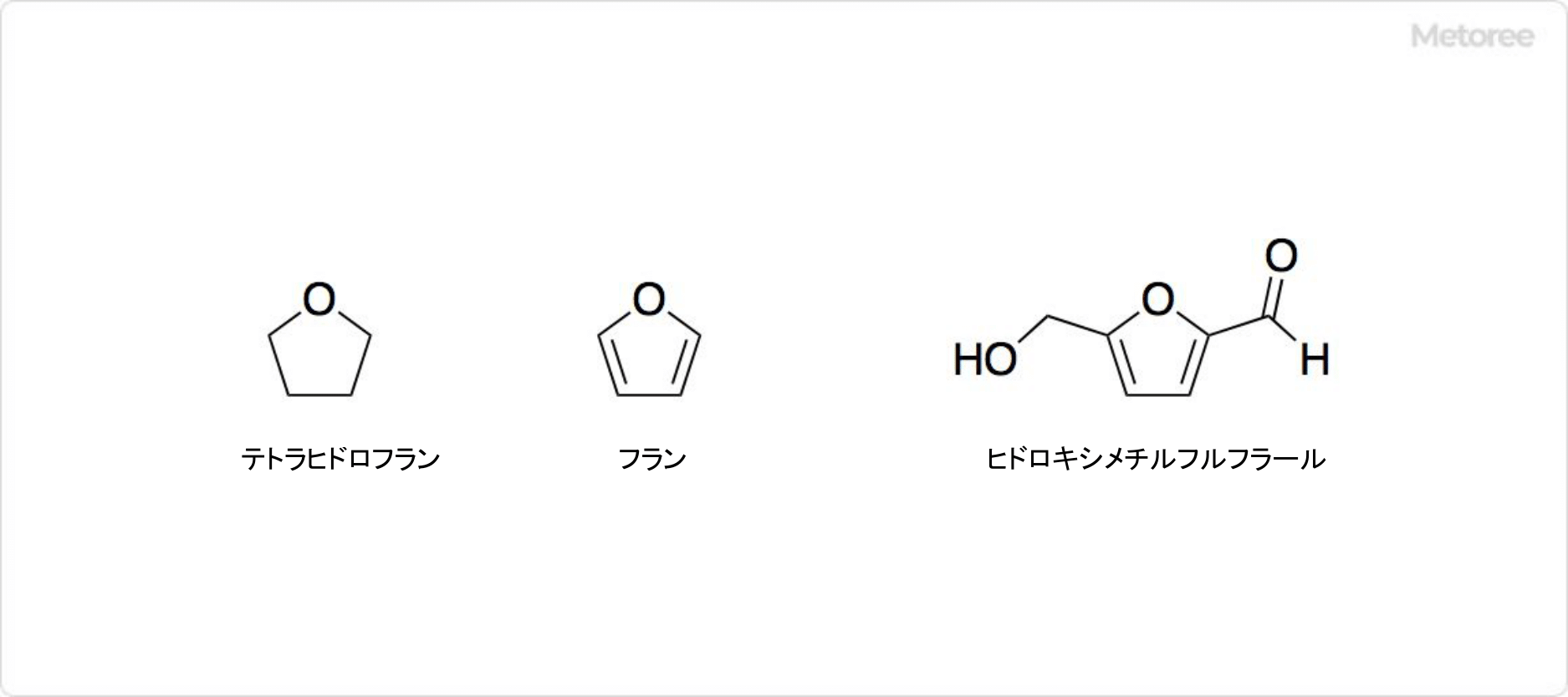
図3. フルフラールの関連化合物
フルフラールは、フランやテトラヒドロフランのような溶剤を製造するための原料です。ヒドロキシメチルフルフラール (英: Hydroxymethylfurfural) の形で、多種多様な加熱食品中にも存在します。ヒドロキシメチルフルフラールは、フルフラールと同じくバイオマスを用いて合成可能です。
フルフラールはフラン樹脂 (英: furan resin) の原料でもあります。アセトン、フェノール、尿素などとともに、フラン樹脂を製造可能です。ナイロンの原料であるアジピン酸 (英: adipic acid) の原料にも利用されています。
3. フルフラールの危険性
フルフラールに触れた際には、気道や皮膚が刺激を受けて、水が肺にたまる場合もあります。フルフラールを吸い込んだり、呑み込んだりした場合には、頭痛、酔い、吐き気、めまい、涙目などの中毒症状を起こす可能性があります。意識不明や死に至るケースもあるため、注意が必要です。