ナフタレンとは
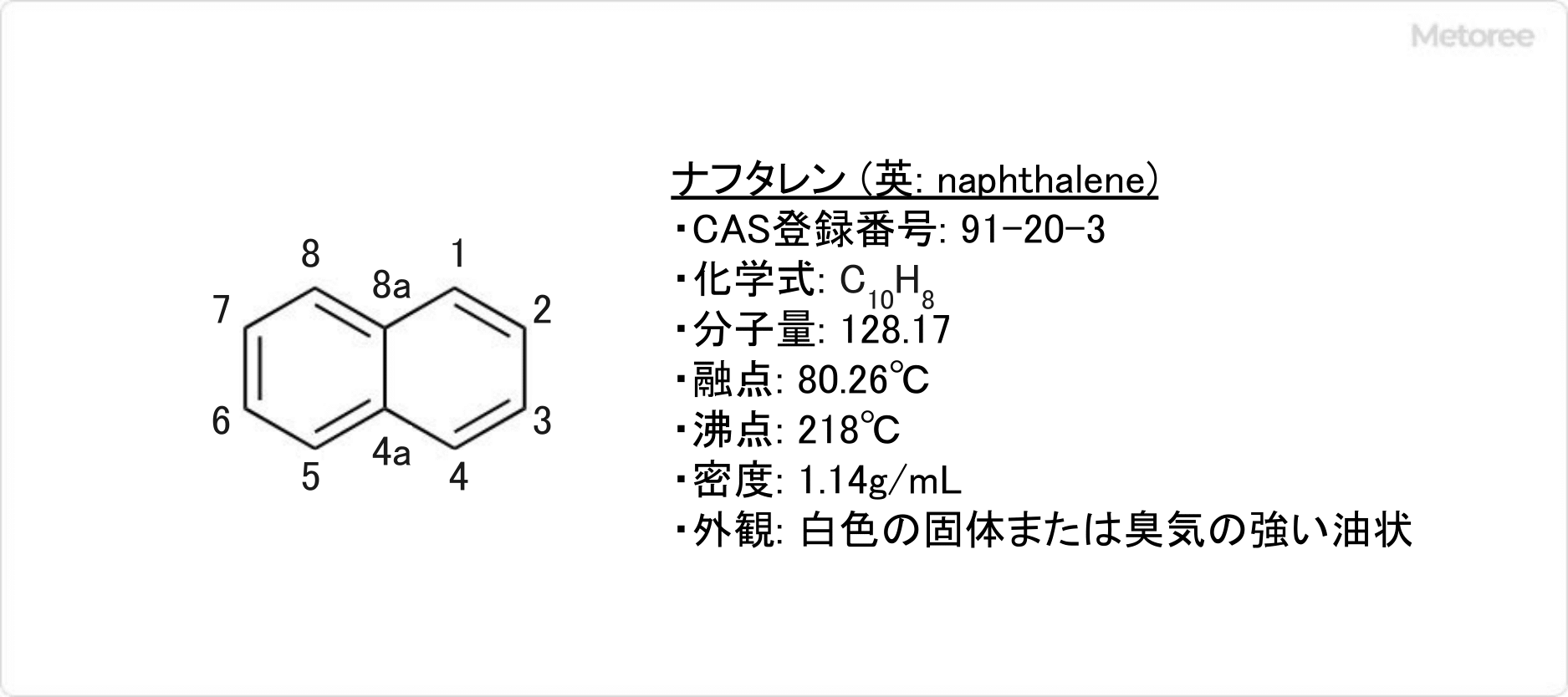
ナフタレンとは、二環式の縮合環を有する芳香族炭化水素の一つです。
ナフタレンは別名、ナフタリンとも呼ばれます。ナフタレンはうろこ状をした白色の結晶です。ナフタレンに紫外線を当てると、紫色の蛍光を発します。スルホン化やニトロ化などの反応の際に、有用な合成中間体です。
ナフタレンは、コールタール中に最も多量に含まれる成分で、コールタールを精製して得られます。コールタールから抽出されたナフタレン油を強制冷却すると、ナフタレンが結晶として析出します。
ナフタレンの使用用途
ナフタレンは室温でも揮発性に優れ、防虫剤や防臭剤として生活に広く使用されています。また、ナフタレンから生成される無水フタル酸は、ポリエステル繊維の原料としても使用可能です。
ナフタレンは、他にも染料中間体や合成樹脂、殺虫剤、滅菌剤、燃料、界面活性剤、ゴムに柔軟性を与える乳化重合用分散剤、有機顔料等の有機化学合成の原料としても幅広く用いられています。
ナフタレンを水素化すると、化学合成やインク塗料等の製造に有用な溶剤であるテトラリンやデカリンを生成可能です。
ナフタレンの性質
ナフタレンには独特の匂いがあり、常温で昇華性を示します。ナフタレンはエタノール、エーテル、ベンゼンなど多くの有機溶剤には溶けますが、水には不溶です。
ナフタレンは2組の等価な水素原子を持っています。α位は1、4、5、8位で、β位は2、3、6、7位です。
ナフタレンの構造
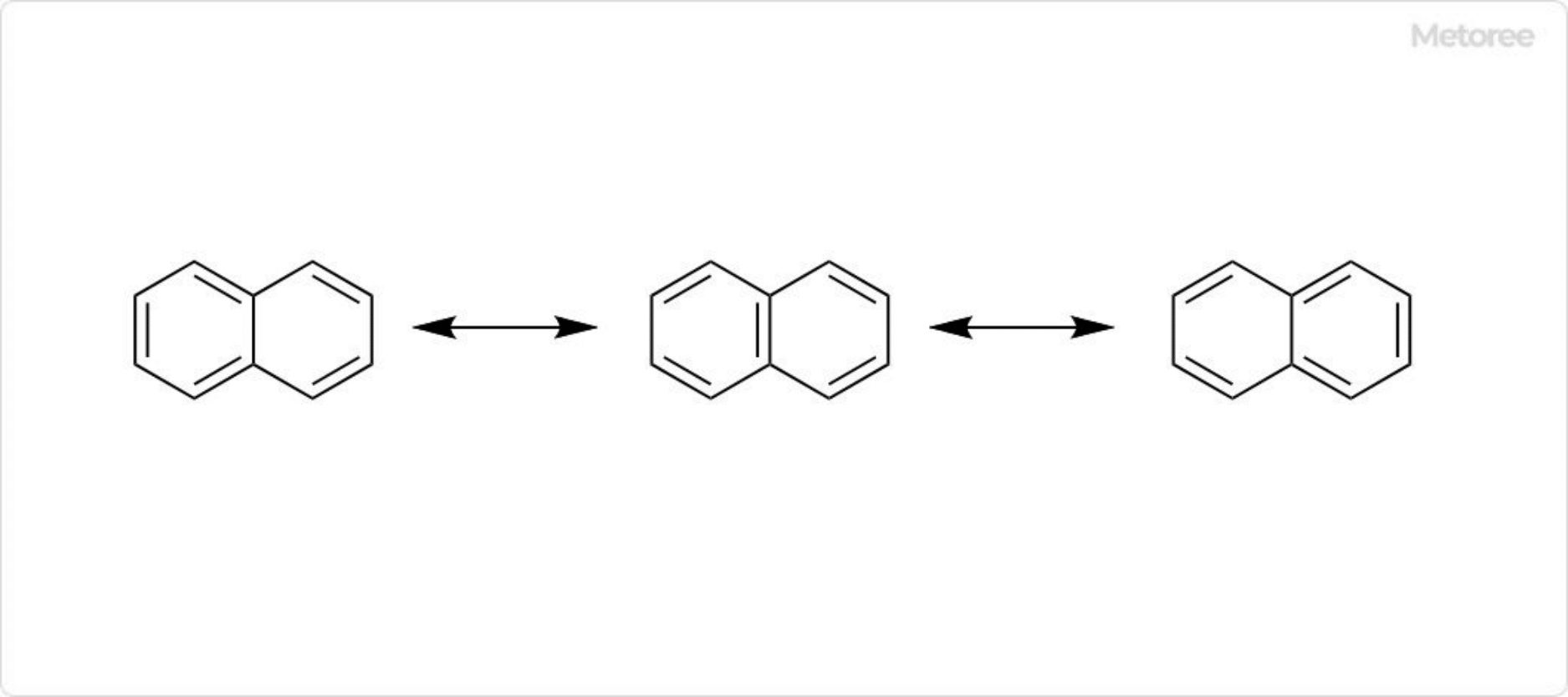
図2. ナフタレンの共鳴構造
ナフタレンは、1辺を2個のベンゼン環が共有している構造を持った多環芳香族炭化水素です。分子式はC10H8、分子量は128.17です。
ナフタレンの炭素-炭素結合は、ベンゼンとは異なり、すべて同じ結合長ではありません。C1-C2、C3-C4、C5-C6、C7-C8間の炭素-炭素結合はおよそ136pmですが、それ以外の炭素-炭素結合の長さはおよそ142 pmです。この違いは3種類の共鳴構造を含めたナフタレン中の結合の原子価結合モデルによって説明できます。
すなわち、C1-C2、C3-C4、C5-C6、C7-C8間の炭素-炭素結合は3種類の共鳴構造のうち2種類が二重結合ですが、それ以外の炭素-炭素結合は共鳴構造のうち1種類のみが二重結合であるためです。
ナフタレンはアセン類 (英: acene) の最も単純な化合物です。ナフタレンの構造異性体には、5員環と7員環で構成されるアズレン (英: azulene) があります。
ナフタレンのその他情報
1. ナフタレンの反応性
ナフタレンもベンゼンと同じように、芳香族求電子置換反応を受けます。ただし、ナフタレンはベンゼンと比べて穏和な条件で反応する場合が多いです。
したがって、ベンゼン上で起きる反応は、ナフタレンでも起こります。位置選択性は反応により違いますが、速度論的に有利なのはα位の置換で、熱力学的に有利なのはβ位の置換です。
2. ナフタレンの置換体
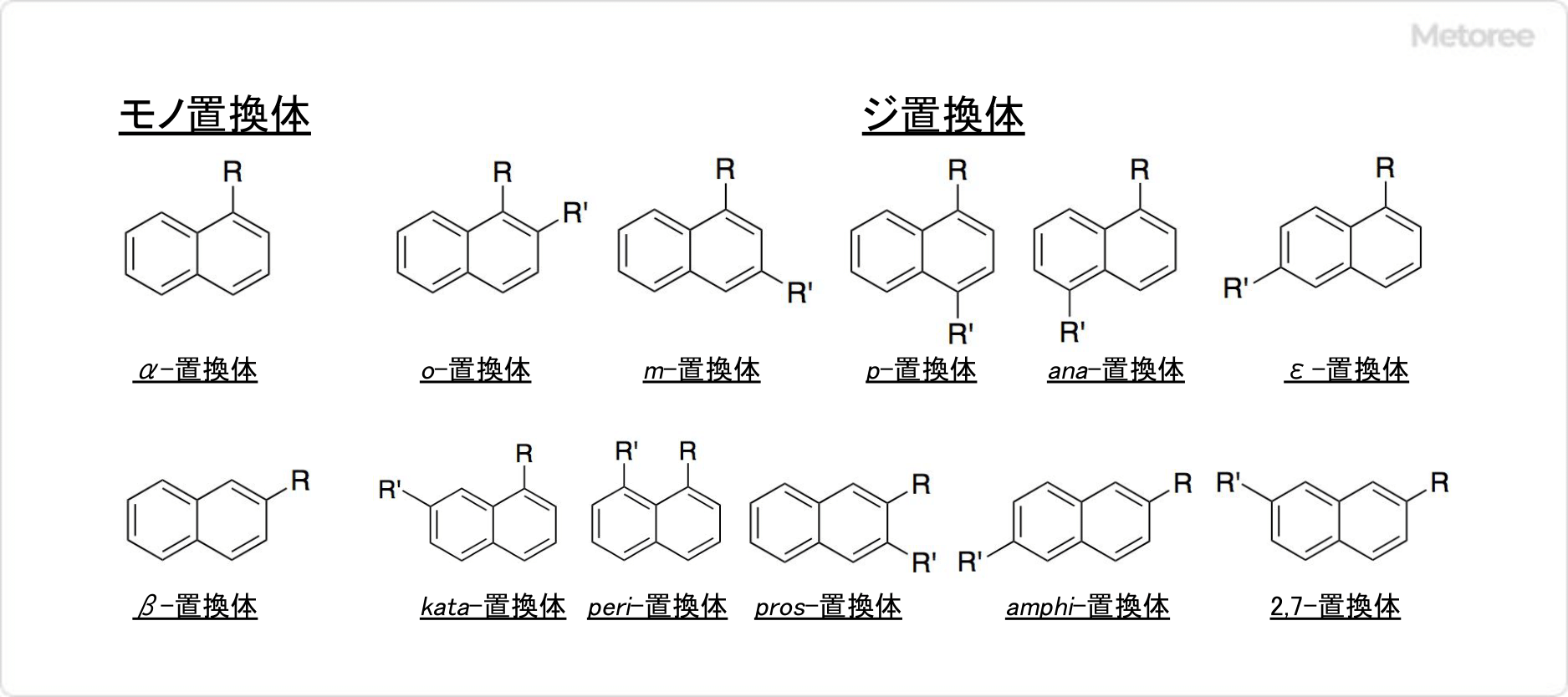
図3. ナフタレンの置換体
ナフタレンにはモノ置換体が2種類、ジ置換体が10種類存在します。2,7位ジ置換体以外には、すべて置換位置を示す接頭辞が付けられています。
1、4、5、8位のモノ置換体は、アルファ (α-) 、2、3、6、7位のモノ置換体は、ベータ (β-) です。1,2位のジ置換体はオルト (o-) 、1,3位のジ置換体はメタ (m-) 、1,4位のジ置換体はパラ (p-) 、1,5位のジ置換体はアナ (ana-) 、1,6位のジ置換体はエピ (ε-) 、1,7位のジ置換体はカタ (kata-) 、1,8位のジ置換体はペリ (peri-) 、2,3位のジ置換体はプロス (pros-) 、2,6位のジ置換体はアンフィ (amphi-) と付けられています。
3. ナフタレンの置換基
ナフタレンから水素を1つ取り去った置換基は、ナフチル基 (英: naphthyl group) と呼ばれています。水素の位置によって、1-ナフチル基と2-ナフチル基が存在します。