Was ist Wolfram?

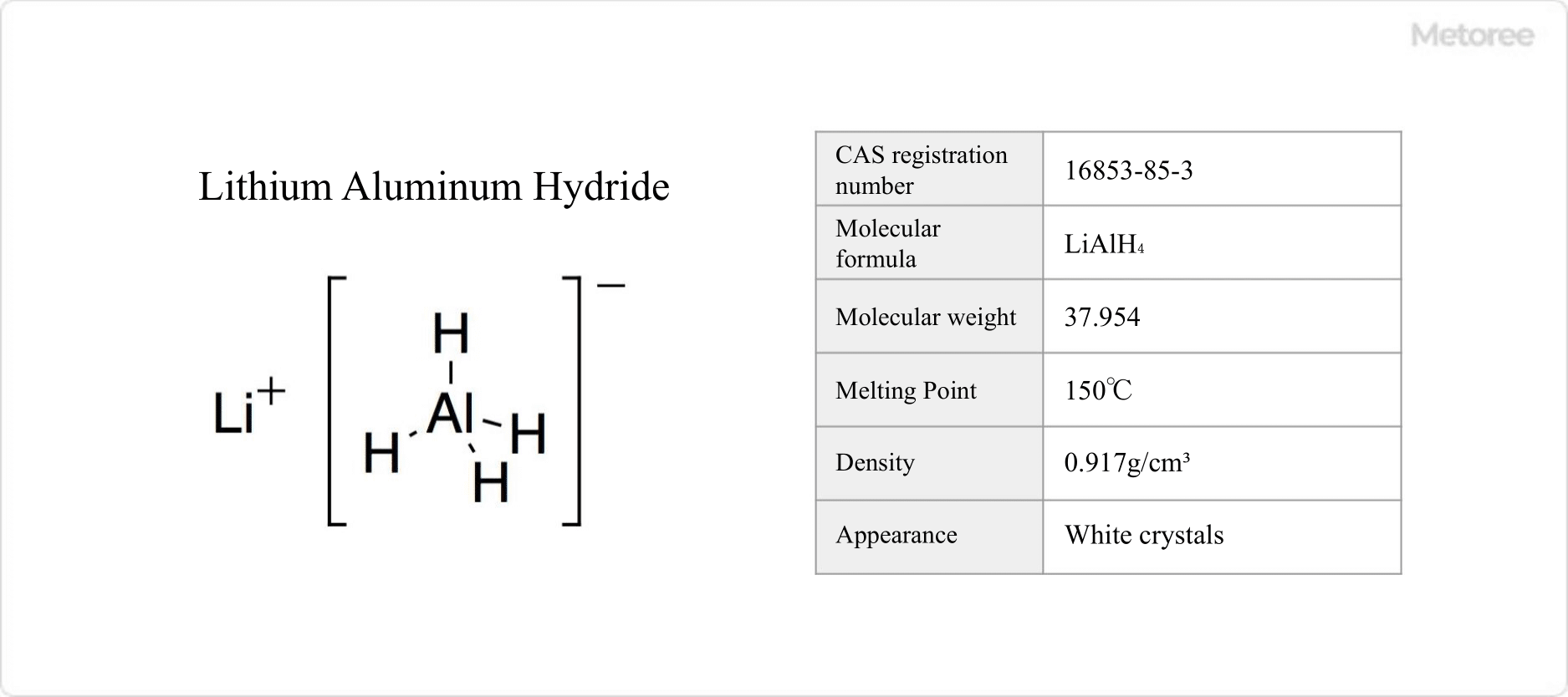
Wolfram (Elementsymbol: W) ist ein Übergangsmetallelement mit einem Atomgewicht von 183,85.
Wolfram wird in verschiedenen Produktformen wie Pulver, Barren, Draht, Stangen und Platten verarbeitet und in verschiedenen Bereichen wie Automobilen, Werkzeugen, Beleuchtung, Haushaltsgeräten, Halbleitern und Medizin verwendet.
Verwendungszwecke von Wolfram
Wolfram wird unter Ausnutzung seiner Eigenschaften für folgende Zwecke verwendet.
- Höchster Schmelzpunkt aller Metalle
Verwendung bei hohen Temperaturen, z. B. als Elektroden zur Erzeugung von Elektronenstrahlen in Elektronenmikroskopen, als Entladungsdrähte und als Elektroden für Entladungslampen
- Relativ hoher elektrischer Widerstand
Glühfäden in Glühbirnen, Ofenheizungen usw.
Wolfram wird auch für Beleuchtungszwecke verwendet, aber seine Verwendung nimmt mit der Verbreitung von LEDs ab. Weitere Anwendungen sind die Verwendung von Wolfram als Legierung mit Kohlenstoff, d. h. eine Legierung aus Wolfram und Kohlenstoff, und Wolfram als Legierung mit Kohlenstoff, d. h. eine Legierung aus Wolfram und Kohlenstoff.
Wolframkarbid, eine Legierung mit Kohlenstoff, ist ein typisches Beispiel. Es ist eine Hartmetalllegierung und wird als Zusatzstoff für Schneidwerkzeuge und Stahl verwendet. Wolframcarbid wird nicht nur für Schneidwerkzeuge, sondern auch als Schleifmittel verwendet, da es bei hohen Temperaturen nicht erweicht, eine hohe Härte beibehält und eine hohe Festigkeit aufweist.
Eigenschaften von Wolfram
Wolfram hat eine silbrig-weiß polierte Masseoberfläche, ein graues Pulver und ein spezifisches Gewicht von 19,3. Es hat den höchsten Schmelzpunkt aller Metalle (3.380°C) und einen Siedepunkt von 5.800°C. Es zeichnet sich außerdem durch einen niedrigen Wärmeausdehnungskoeffizienten aus und wird als Rohstoff für Behälter und Bauteile verwendet, die bei hohen Temperaturen eingesetzt werden, wie Tiegel und Öfen.
Obwohl Wolfram nicht der Hauptbestandteil ist, wurde eine Eisenlegierung, die Kobalt, Wolfram, Chrom und Kohlenstoff enthält und als KS-Stahl bekannt ist, als der stärkste Dauermagnet bezeichnet, als sie 1917 in Japan entwickelt wurde.
Wolfram-Erz wird mit anderen Metallen wie Wolframit, Ferranit, Mangan-Hubnerit, Scheelit und CaWO4 vermischt. Ferromangan-Schwarzerz und Asche-Schwarzerz sind die wichtigsten Erze.
Mehr als 80 % der Erze werden in China gefördert, die übrigen in Russland, Australien und Kanada. Trotz der ungleichmäßigen Produktion ist Wolfram ein sehr wichtiges Element, und die Sicherheitsmaßnahmen sehen vor, dass für den Inlandsverbrauch Vorräte für mindestens 60 Tage angelegt werden müssen.
Weitere Informationen über Wolfram
1. Arten von Wolframlegierungen
Es wurde eine Reihe von Wolfram-Legierungen entwickelt, und Sinterlegierungen auf Wolfram-Basis mit einer Bindephase aus Nickel, Kupfer oder Eisen werden als Schwerlegierungen bezeichnet. Zu den Schwermetalllegierungen gehören die Systeme Wolfram-Nickel-Kupfer (W-Cu-Ni) und Wolfram-Nickel-Eisen (W-Fe-Ni).
Das Wolfram-Nickel-Kupfer-System ist nicht magnetisch, aber ein guter Wärmeleiter. Das Wolfram-Nickel-Eisen-System hingegen ist schwach magnetisch und hat hervorragende mechanische Eigenschaften wie Zugfestigkeit und Dehnung. Schwere Legierungen werden durch Pulvermetallurgie hergestellt, da Wolfram einen sehr hohen Schmelzpunkt hat.
Bei der Herstellung wird das Metallpulver gleichmäßig gemischt, unter hohem Druck gepresst und anschließend bei hohen Temperaturen gesintert. Die physikalischen Eigenschaften der Legierung lassen sich durch die Einstellung der Partikelgröße des bei der Herstellung verwendeten Wolframs, der Art des als Bindemittel verwendeten Metalls und des Mengenverhältnisses differenzieren.
2. Toxizität von Wolfram
Da Wolfram-Barren selbst ungiftig sind, können sie in Anwendungen mit direktem Kontakt wie Werkzeugen und Zubehör verwendet werden. Andererseits wird der bei der Wolframverarbeitung entstehende Wolframstaub in der Klassifizierung der Staubgefährdungsstufen der Japan Society for Occupational Health als Staub der Klasse III eingestuft, und die maximal zulässige Staubmenge in der Arbeitsumgebung ist festgelegt.
Was die Toxizität von Wolframverbindungen betrifft, so liegen die Werte für die halbtödliche Dosis LD50 (ein Indikator für akute Toxizität) bei oraler Aufnahme durch Ratten bei 3.300 mg/kg für Phosphowolframsäure, 1.190 mg/kg für Natriumwolframat und 840 mg/kg für Wolframoxid (VI). Die Toxizität dieser Verbindungen ist nicht bekannt.
Keine dieser Verbindungen fällt unter das Gesetz zur Kontrolle giftiger und schädlicher Stoffe, aber nach dem Gesetz über Gesundheit und Sicherheit am Arbeitsplatz werden sie als gefährliche und gefährliche Stoffe eingestuft, die namentlich gekennzeichnet und gemeldet werden müssen.