亜硫酸とは
亜硫酸 (英: Sulfurous acid) とは、二酸化硫黄の水溶液中に存在すると考えられている、化学式H2SO3で表される酸です。
硫黄のオキソ酸の1つに分類される物質であり、CAS登録番号は7782-99-2です。ただし、遊離酸は不安定であるため、単離はできません。かつては水溶液中にH2SO3の状態で含有されていると考えられていましたが、実際は亜硫酸水素イオンHSO3–が生じていると考えられています。
多くは亜硫酸水の状態で販売されており、また二硫化硫黄 (英: Sulfur dioxide) の気体を亜硫酸ガスと呼ぶ場合もあります。
亜硫酸の使用用途
亜硫酸、及び、二酸化硫黄は、還元剤・漂白剤として用いられる物質です。食品添加物としてとしての用途があり、ドライフルーツや酒の保存料、漂白剤、酸化防止剤として使われています。
その他の産業用途では、殺菌剤 (食品加工、器具の消毒など)、農業用くん蒸剤、殺虫剤、消毒剤、防腐剤、保存剤 (果物及び野菜の防腐) を挙げることができます。製紙、繊維及び織物、麦わら、ゼラチン、グルー、てん菜糖の漂白剤としても使用されている物質です。
亜硫酸の性質

図1. 亜硫酸の基本情報
亜硫酸/亜硫酸水は、水と二酸化硫黄の混合物として扱われます。無色の澄明な液体で、密度は1.03g/mLです。刺激臭を有し、水やエタノールと任意で混和します。
亜硫酸の種類
1. 亜硫酸水
亜硫酸水は通常研究開発用試薬製品として販売されています。主な想定用途は一般分析用試液、還元剤などです。
濃度は二酸化硫黄の濃度で5%や6%程度が多く、容量の種類は、100g、500g、2kg、500mLなどです。通常室温で保管可能な試薬製品として扱われますが、二酸化硫黄臭が強いのでドラフト中で取り扱うこととされます。
2. 亜硫酸ガス
産業用製品の中には、二酸化硫黄のガス製品を亜硫酸ガスと呼んでいるものがあります。漂白剤、還元剤、金属製造用、工業薬品製造用などに用いられますが、通常高圧ガス・液化ガスであるため、安全な取り扱いには注意が必要です。
亜硫酸のその他情報
1. 亜硫酸水の平衡
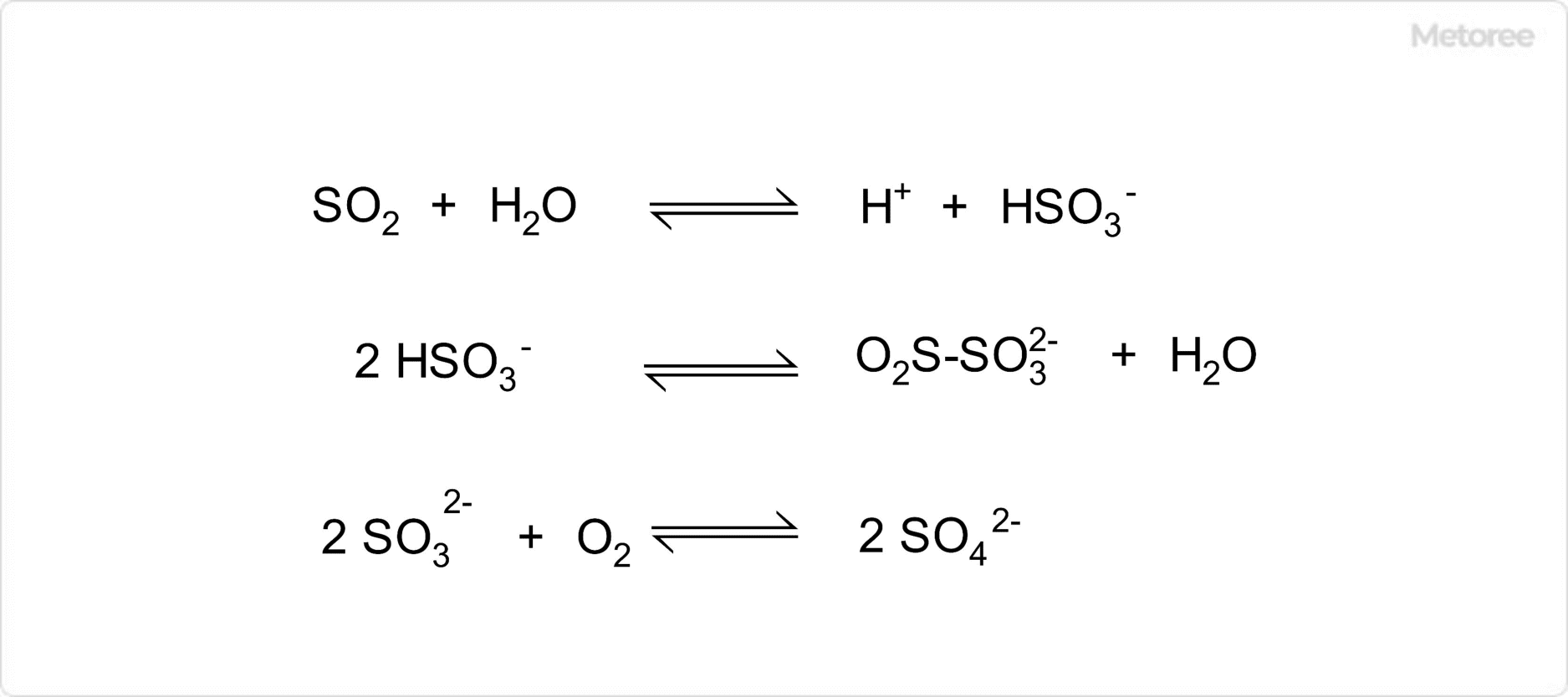
図2. 亜硫酸水の平衡
かつては亜硫酸水には亜硫酸H2SO3が溶解していると考えられていましたが、今日では亜硫酸水素イオン、亜硫酸イオンがそれぞれ平衡状態にあると考えられています。
さらに、水溶液中では、亜硫酸水素イオンは2量化した構造との平衡にあると考えられており、亜硫酸イオンは溶液中の酸素と反応して生じる硫酸イオンとの平衡関係にあると考えられています。
2. 亜硫酸の物理的危険性
亜硫酸や二酸化硫黄は、加熱によって、破裂の危険を伴う圧力の上昇が起こり危険があります。水溶液は中程度の強酸で、アンモニア、アクロレイン、アセチレン、アミン類、アルカリ金属類、塩素、酸化エチレン、ブタジエンと激しく反応します。
また、水や水蒸気とは反応して腐食の危険をもたらす物質です。ハロゲンとの接触にも注意が必要となります。
3. 亜硫酸の人体への有害性
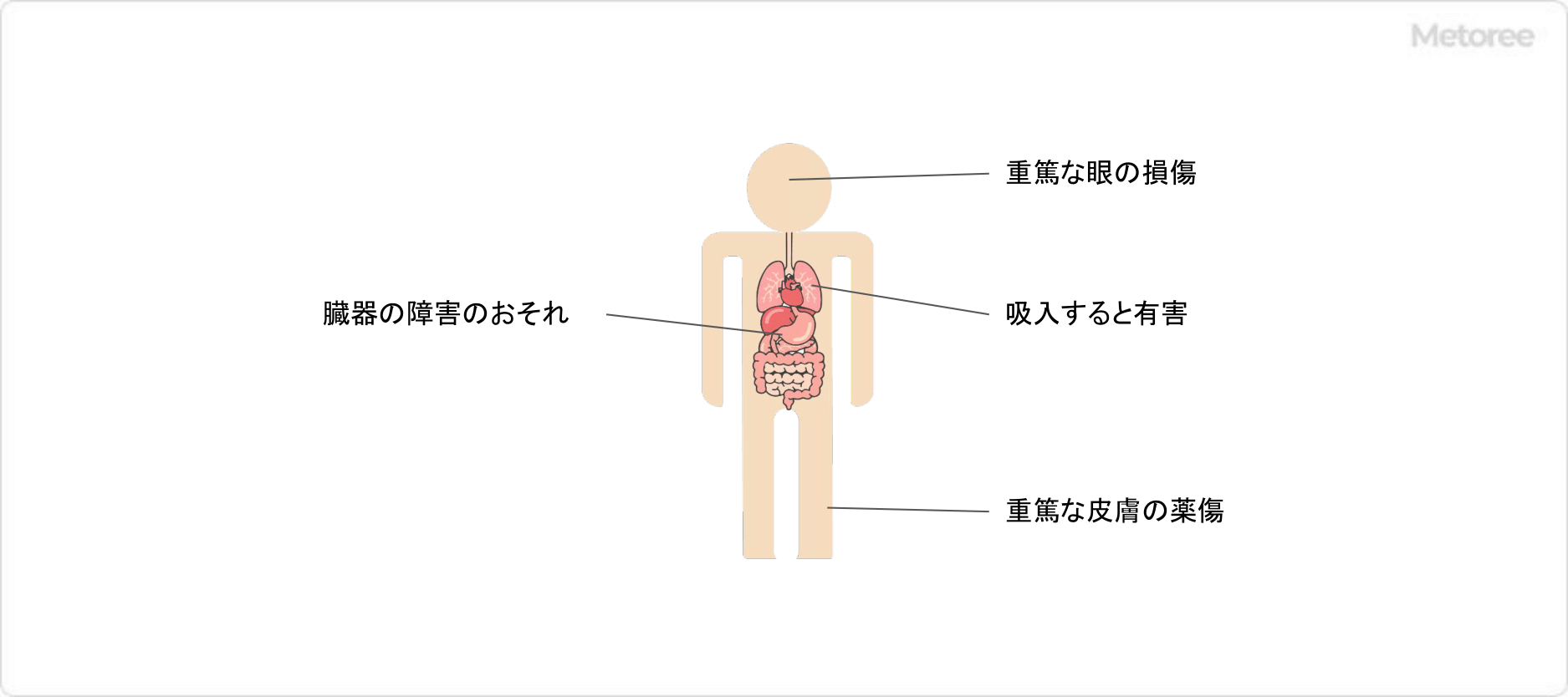
図3. 亜硫酸の人体への有害性
亜硫酸は、人体への有害性のある物質です。具体的には、以下の危険性が指摘されています。
- 重篤な皮膚の薬傷
- 重篤な眼の損傷
- 吸入すると有害
- 臓器の障害のおそれ
- 長期にわたる、又は反復ばく露による臓器の障害のおそれ
また、GHS分類では下記のように分類されています。
- 急性毒性-吸入 (蒸気) : 区分4
- 皮膚腐食性/刺激性: 区分1
- 眼に対する重篤な損傷性/眼刺激性: 区分1
- 特定標的臓器毒性 (単回ばく露) : 区分2
- 特定標的臓器毒性 (反復ばく露) : 区分2
4. 亜硫酸の法規制情報
亜硫酸は、前述の有害性のため法令で規制を受ける物質です。労働安全衛生法において、特定化学物質第3類物質、名称等を表示すべき危険物及び有害物、名称等を通知すべき危険物及び有害物に指定されています。
法令を遵守して正しく取り扱うことが必要です。
参考文献
http://www.etosanso.co.jp/sds/pdf/sds027.pdf
https://www.ilo.org/dyn/icsc/showcard.display?p_lang=ja&p_card_id=0074&p_version=2