ヨウ化亜鉛とは
ヨウ化亜鉛 (英: Zinc iodide) とは、化学式ZnI2であらわされる、亜鉛のヨウ化物です。
CAS登録番号は10139-47-6です。無水和物の他、二水和物が存在します。どちらも潮解性のある物質です。
ヨウ化亜鉛の使用用途
ヨウ化亜鉛の主な使用用途は、放射線の遮蔽、ヨウ化亜鉛でんぷん指示薬の原料、シモンズ・スミス反応の試薬、歯科治療での殺菌剤、電子材料などです。
ヨウ化亜鉛でんぷん指示薬は、亜硝酸、塩素などの酸化剤によって青色を呈色するため、これら酸化剤の検出試薬として用いられています。また、ヨウ化亜鉛を試薬として用いるシモンズ・スミス反応は、オレフィンをシクロプロパン化する反応であるため、シクロプロパン環を有する生理活性物質や医薬品などの合成に有用な反応を示します。
ヨウ化亜鉛の性質

図1. ヨウ化亜鉛の基本情報
ヨウ化亜鉛の式量は319.218、融点446℃、沸点624℃ (分解) であり、常温での外観は、白色から黄褐色の結晶性粉末、または塊の物質です。
密度は4.74g/mLであり、水やエタノールに容易に溶解する性質があります。水への溶解度は、333g/100mlであり、また潮解性のある物質です。
光により変質するおそれがあり、直射日光と高温を避けて保管することが必要です。酸類とは反応するため、混触を避けるべきとされます。分解によってハロゲン化物 (ヨウ化物) や金属酸化物を生じる物質です。
ヨウ化亜鉛の種類
ヨウ化亜鉛は、主に研究開発用試薬製品や、産業用材料として販売されている物質です。試薬製品としては、25g、50g、250gなど実験室で取り扱いやすい容量の種類があります。通常、室温で保管可能な試薬製品としての提供です。
また、純粋な物質以外では、ヨウ化亜鉛でんぷん溶液としても販売されています。こちらは、100mLなどの単位での販売です。
産業用途では電子材料などとして提供されています。容量の種類は5kgなど、試薬製品よりはやや大型容量からの提供になります。
ヨウ化亜鉛のその他情報
1. ヨウ化亜鉛の合成法
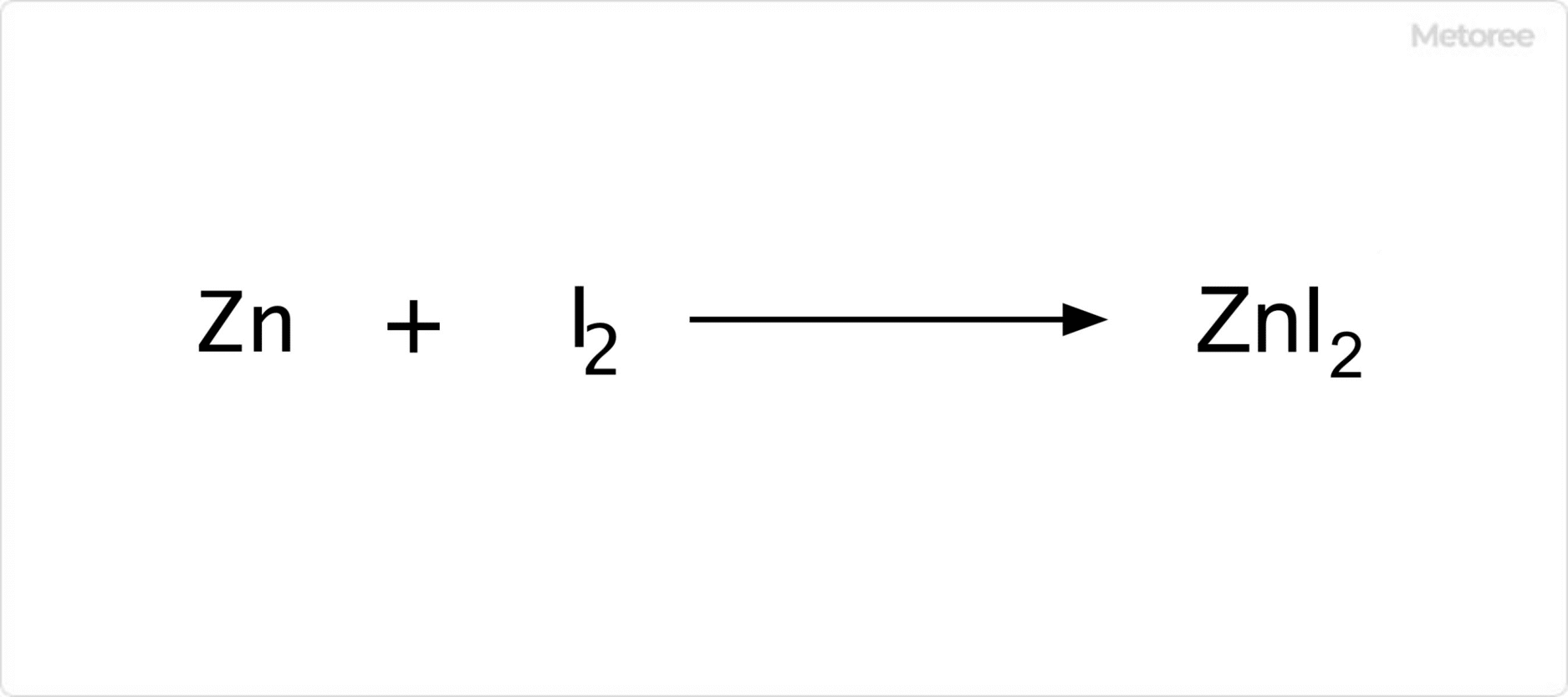
図2. ヨウ化亜鉛の合成
ヨウ化亜鉛の製造方法は、金属亜鉛とヨウ素を高温で反応させる方法や、亜鉛末とヨウ素の混合物に水を滴下して得られたヨウ化亜鉛水溶液を蒸発濃縮する方法などが知られています。
実験室的製法では、水中若しくはエーテル溶液加熱還流下で亜鉛とヨウ素を反応させることが一般的です。
2. ヨウ化亜鉛の化学反応
ヨウ化亜鉛は水溶液中では、Zn(H2O)62+、 [ZnI(H2O)5]+、 ZnI2(H2O)2、ZnI3(H2O)−、ZnI42−などの分子種を生じることが知られています。ルイス酸として、種々の有機合成反応に用いられている物質です。
また、シモンズ・スミス反応の変法として、ジアゾメタンとヨウ化亜鉛を反応させ、系中で活性種であるICH2ZnI を発生させる方法があります。
3. シモンズ・スミス反応

図3. シモンズ・スミス反応
シモンズ・スミス反応とは、ジハロアルカンによりアルケンをシクロプロパン化する化学反応です。反応活性種は、亜鉛にジヨードメタンが酸化的付加して生成する ICH2ZnI (カルベノイドの1種) という分子であり、2つのσ結合が協奏的に生成してシクロプロパン環が生成すると考えられています。
活性種であるICH2ZnIの主な調製方法は、下記の通りです。
- 亜鉛–銅カップルの存在下、アルケンにエーテル系溶媒中でジヨードメタンを加える
- 上記方法の変法で、亜鉛の代わりにEt2Zn、 Cu、 R3Al, Sm(Hg)などを用いる
- CH2N2-ZnI2系試剤を用いる
なお、ヨウ化亜鉛は、シモンズ・スミス反応の副生成物でもあります。
4. ヨウ化亜鉛の有害性
ヨウ化亜鉛は、GHS分類において、経口摂取による急性毒性が認められており、有害性のある物質です。ヨウ化亜鉛は、毒物及び劇物取締法において、劇物に指定されており、労働安全衛生法においては、名称等を表示すべき危険物及び有害物や、名称等を通知すべき危険物及び有害物に指定されています。
引火性はないため消防法での規制はありませんが、PRTR法では第1種指定化学物質に指定されています。取り扱いの際は法令を遵守して正しく取り扱うことが必要です。
参考文献
https://labchem-wako.fujifilm.com/sds/W01W0126-0106JGHEJP.pdf