亜硫酸水素ナトリウムとは
亜硫酸水素ナトリウムとは、化学式NaHSO3で表される無機化合物です。
通常は、亜硫酸水素ナトリウム (NaHSO3) と重亜硫酸ナトリウム (ピロ亜硫酸ナトリウム (Na2Ss2O5)) との混合物です。別名として、重亜硫酸ソーダ、酸性亜硫酸ソーダ、無水重亜硫酸ソーダなどがあります。
わずかに硫黄臭のある白い単結晶の粉末で、水に溶けやすく、エタノールにはほとんど溶けません。水溶液は弱酸性を示します。
亜硫酸水素ナトリウムの使用用途
亜硫酸水素ナトリウムは、食品添加物の防腐剤、漂白剤として広く使用されています。その他にも、皮革 (タンニン溶解剤) 、染料及び中間物精製、写真 (定着補助剤) 、還元剤、漂白剤、廃液処理剤、洗剤、香料、試薬、医薬化粧品原料 (抗酸化剤) と使用用途は様々です。化粧品原料として使用する場合は、製品中への配合量の上限が定められています。
また、化学物質過敏症やシックハウス症候群の原因物質の一つとされているホルムアルデヒドと亜硫酸塩、重亜硫酸塩は水分の存在下で反応し、分子内に取り込むことができるため、ホルムアルデヒドが空気中に放散することを抑制するアルデヒドキャッチャーとしても使用されています。
亜硫酸水素ナトリウムは、刺激性があり、健康への影響も懸念されるため、用途によってそれぞれの配合量上限が定められいる点に注意が必要です。
亜硫酸水素ナトリウムの性質
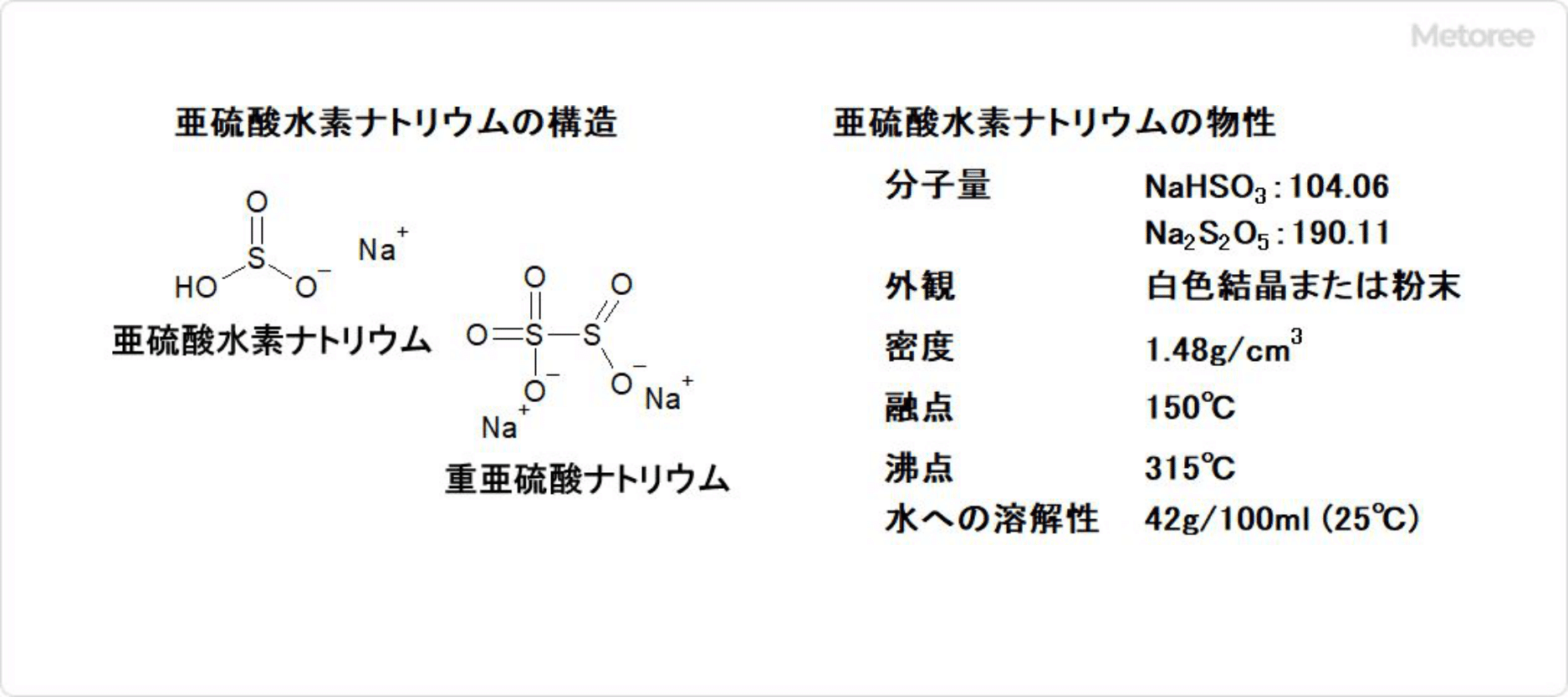
図1. 亜硫酸水素ナトリウムの構造と物性
亜硫酸水素ナトリウム (亜硫酸水素ナトリウムと重亜硫酸ナトリウムの混合物) の分子構造は、亜硫酸水素イオンと重亜硫酸イオンそれぞれがナトリウムイオンと塩を形成したものです。室温においてさえ、固体の状態では不安定で、空気中で徐々に酸化され、微量の亜硫酸ガスを放ちながら硫酸塩に変化します。
そのため、製品形態としては粉末状の固体としてだけではなく、34%以上の高濃度水溶液としても販売されています。水溶液は加熱すると分解し、アルデヒドと付加物を作ります。
亜硫酸水素ナトリウムのその他情報
1. 亜硫酸水素ナトリウムの製造方法
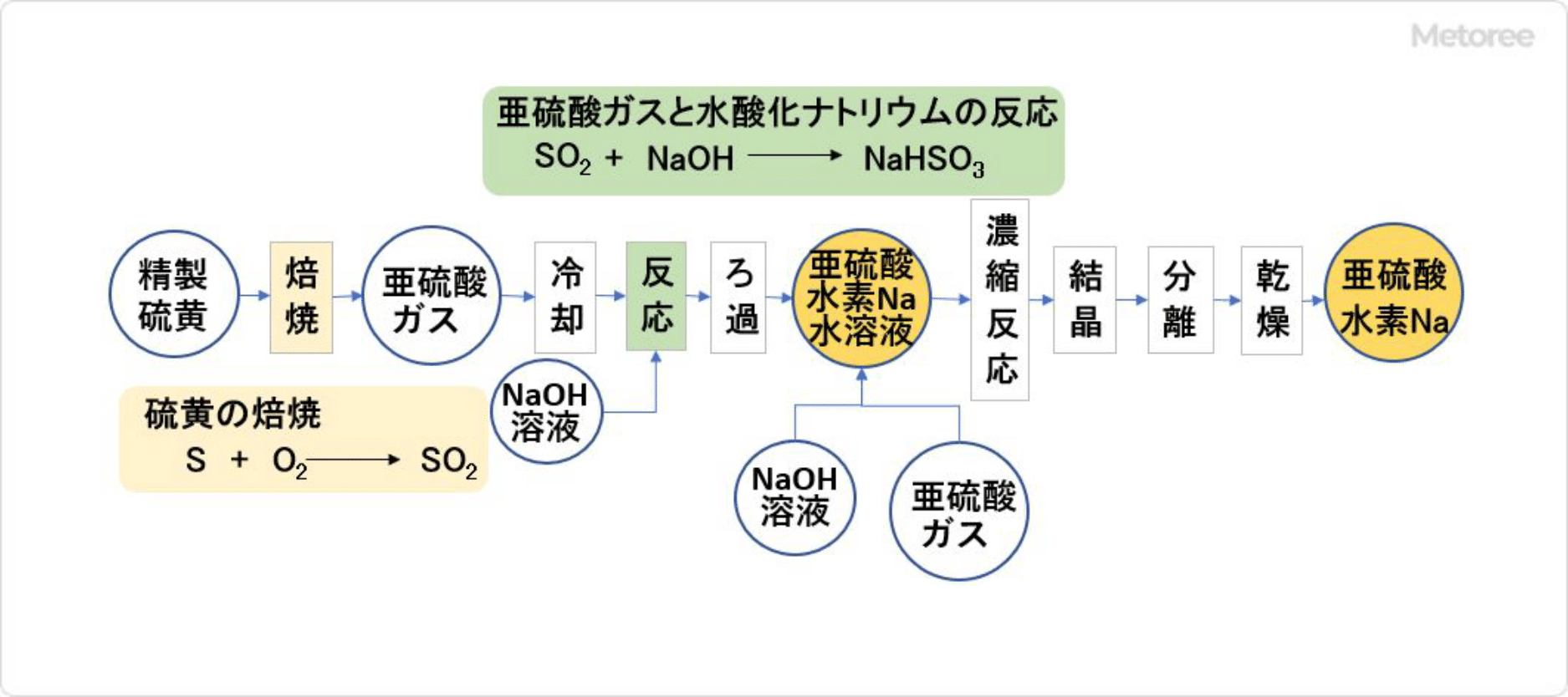
図2. 亜硫酸水素ナトリウムの製造方法
原料としては精製硫黄 (S) と水酸化ナトリウム (NaOH) を使用します。精製硫黄を焙焼 (空気の存在下で高温に加熱) することで、亜硫酸ガスを生成させます。吸収槽中で水酸化ナトリウム水溶液に亜硫酸ガスを吹き込むと、淡黄色透明の反応液が得られます。この反応液を濾過することで亜硫酸水素ナトリウム水溶液が得られます。
亜硫酸水素ナトリウム水溶液に、追加で水酸化ナトリウム水溶液と亜硫酸ガスを加えることで、さらに濃厚な亜硫酸水素ナトリウム水溶液に濃縮可能です。これを冷却、ろ過することで亜硫酸水素ナトリウムの結晶を得ることができます。
亜硫酸水素ナトリウムの結晶を乾燥加熱すると脱水反応が起こり、重亜硫酸ナトリウムの無色粉末になりますが、これを水に溶解させると再び亜硫酸水素ナトリウムに戻ります。
2. 亜硫酸水素ナトリウムの安全性

図3. 亜硫酸水素ナトリウムの安全性と法規制
亜硫酸水素ナトリウム自体は不燃物ですが、高温で熱分解すると亜硫酸ガス (二酸化硫黄) の有害ガスが発生します。酸、鉱酸類などとの反応によっても亜硫酸ガスを発生します。また、酸化剤との混合により激しく発熱します。
労働安全衛生法では、名称等を表示すべき危険物及び有害物およびリスクアセスメントを実施すべき危険有害物に該当します。それ以外の法令においても有害物質、腐食性物質など危険性の高い種類の化合物として指定されており、取扱いには注意を要します。
参考文献
https://labchem-wako.fujifilm.com/sds/W01W0119-0137JGHEJP.pdf