亜塩素酸とは
亜塩素酸 (英: Chlorous acid) とは、化学式HClO2で表される塩素のオキソ酸の1種です。
CAS登録番号は13898-47-0です。塩素の酸化数は+3あり、塩素酸 (+5価) よりも酸化数が小さいため、亜塩素酸と呼ばれます。遊離酸としては非常に不安定であるため、基本的には水溶液として存在します (亜塩素酸水) 。
なお、亜塩素酸塩は常温で安定です。具体的なものには亜塩素酸ナトリウム (NaClO2) や亜塩素酸カリウム (KClO2) などがあります。
亜塩素酸の使用用途
亜塩素酸の水溶液である「亜塩素酸水」の主な使用用途は、殺菌消毒剤です。細菌類等に対する殺菌効果やウイルス類の不活化効果が認められています。塩素のオキソ酸の中では、消毒剤として良く知られる次亜塩素酸より酸性度・酸化力が強く、塩素酸よりは弱いです。
亜塩素酸水は、食品添加物の製造用剤 (殺菌料) として認可されていますが、最終食品の完成前に除去あるいは分解しなければならないとされる物質です。具体的には、「精米、豆類、 (きのこ類を除いた) 野菜、果実、海藻類、鮮魚介類、食肉、食肉製品及び鯨肉製品並びにこれらを塩蔵、乾燥その他の方法によって保存したもの」などに対して使用が認められています。
亜塩素酸の性質
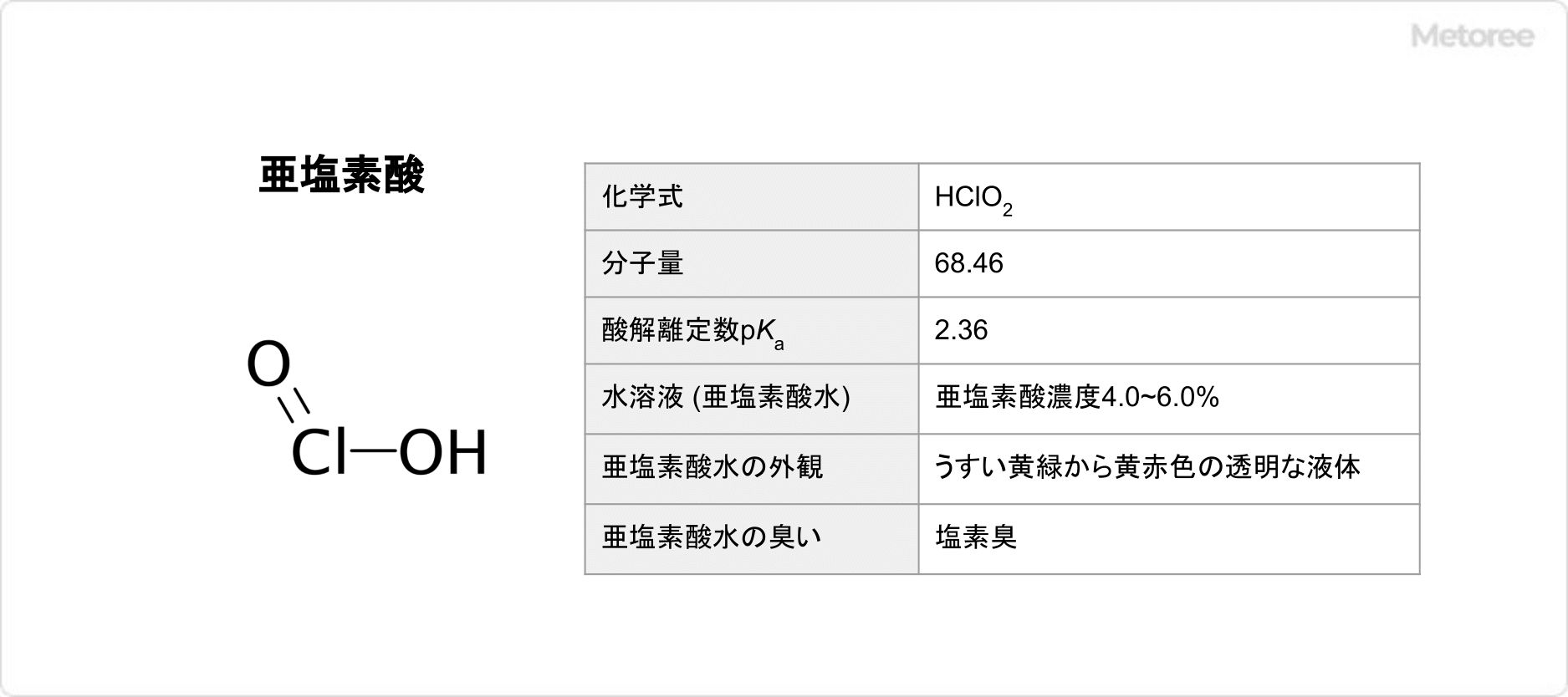
図1. 亜塩素酸の基本情報
亜塩素酸HClO2は、分子量68.46、酸解離定数pKaは2.36である、中程度の酸です。また、亜塩素酸水は、亜塩素酸を4.0~6.0%程度含む水溶液で、うすい黄緑から黄赤色の透明な液体です。塩素の臭いを帯びます。
亜塩素酸水は、亜塩素酸 (HClO2) 分子の状態で存在していることはほとんどありませんが、瞬間的に存在する非解離状態の亜塩素酸 (HClO2) と解離状態の亜塩素酸イオン (H+・ClO−2) が平衡状態にあると考えられています。
亜塩素酸の種類
亜塩素酸水は、主に食品添加物として販売されている他、あるいはその他の物質と混合した殺菌消毒液として販売されています。また、関連物質として亜塩素酸の塩である、亜塩素酸ナトリウムや亜塩素酸カリウムなどが販売されています。
こちらは常温で安定な物質であることから、有機合成などに用いられる研究開発用試薬製品や、一般的な漂白剤薬品などとして広く販売されている物質です。
亜塩素酸のその他情報
1. 亜塩素酸の合成
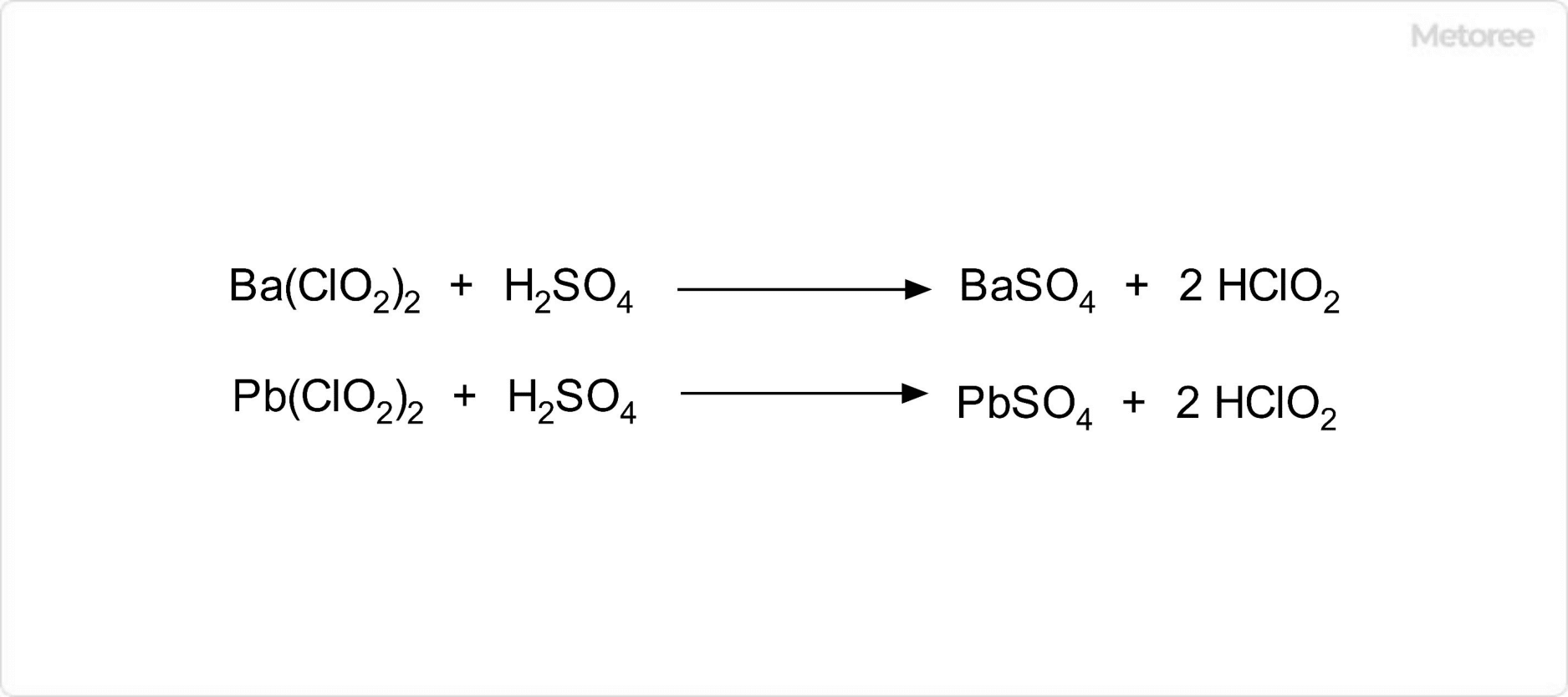
図2. 亜塩素酸の合成
遊離酸としての亜塩素酸は、亜塩素酸バリウムや亜塩素酸鉛などの水溶液に硫酸等の強酸を加え、生じた沈殿を濾別することで得られます。ただし、室温では容易に分解して二酸化塩素と次亜塩素酸となるため、低温下で合成・精製することが必要です。
2. 亜塩素酸水の合成
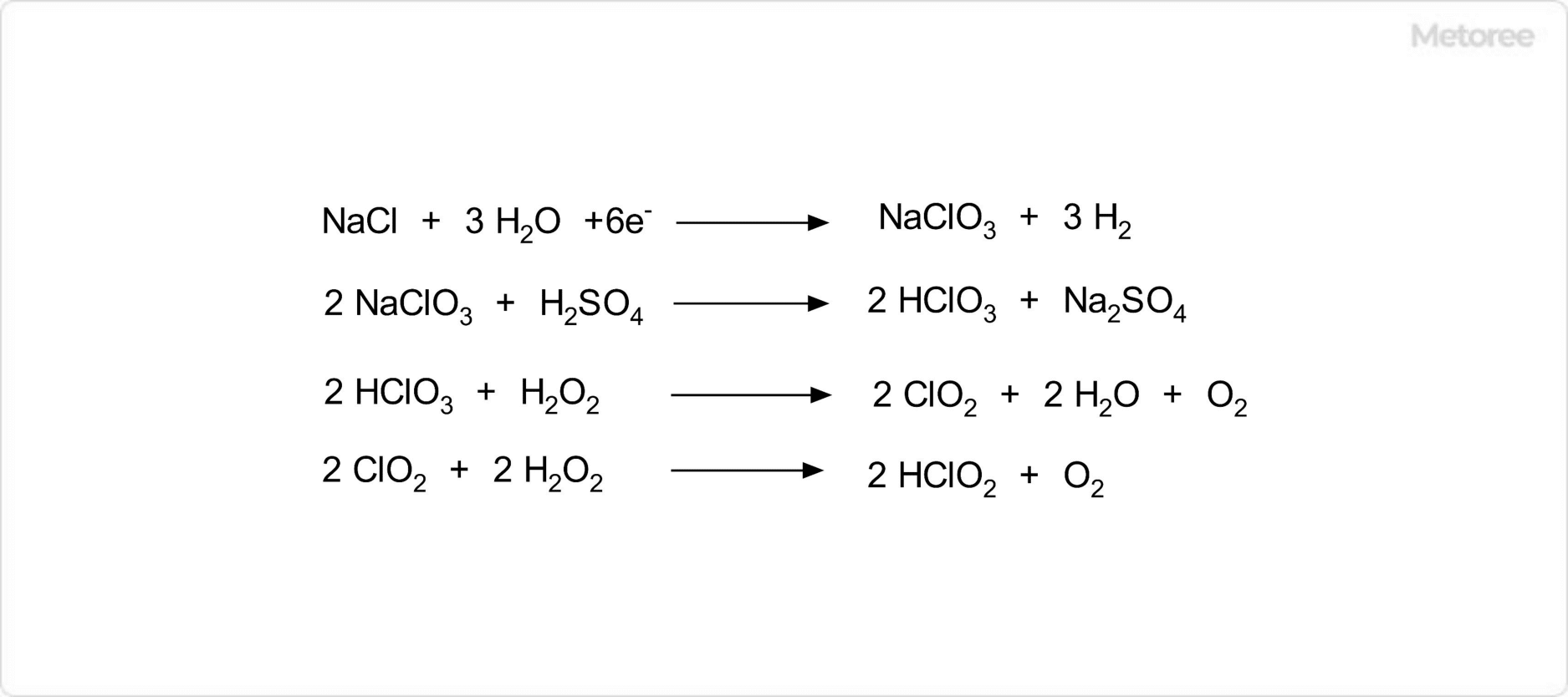
図3. 亜塩素酸水の合成
亜塩素酸水は、下記の合成手順で合成される物質です。
- 飽和塩化ナトリウム溶液に塩酸を加え、酸性条件下で、
無隔膜電解槽内で電解する - 得られた水溶液に、硫酸を加えて強酸性とする
- 生成した塩素酸に過酸化水素水を加えて反応させる
その他、亜塩素酸ナトリウムにGRAS酸を加えても亜塩素酸 (HClO2) は生じるものの、この方法で合成された亜塩素酸は容易に分解され、安定に存在させる事はできません。前述の合成方法は亜塩素酸を液中に安定化させる優れた方法であるとみなされています。
3. 亜塩素酸の化学反応
亜塩素酸は不安定なため、不均化により、次亜塩素酸 (HClO) と塩素酸 (HClO3) を発生させます。酸化作用があり、有機合成では反応系中で亜塩素酸を発生させて酸化剤として用いる場合があります。
具体的な例としては、アルデヒドをカルボン酸へ酸化する反応などが挙げられます。この反応では、リン酸緩衝液などで pH を微弱な酸性に保った状態で行われることが多いです。
また、次亜塩素酸 (HClO) など、副反応を誘発する塩素化合物が発生するため、これらを捕捉するために、捕捉剤 (2-メチル-2-ブテンなど) がしばしば添加されます。
参考文献
https://www.mhlw.go.jp/stf/shingi/2r9852000002wy32-att/2r9852000002wybn.pdf