シアン化カリウムとは
シアン化カリウムとは、化学式KCNで表される無機化合物で、青酸カリウム、青酸カリとも呼ばれます。常温では無色の結晶性塩として見られ、水に良く溶けます。
強い毒性を持つことから毒物の代名詞になっていますが、有機合成、金の製錬、電気めっきなど広い分野で実用に供されている工業的に重要な物質でもあります。
シアン化カリウムの性質
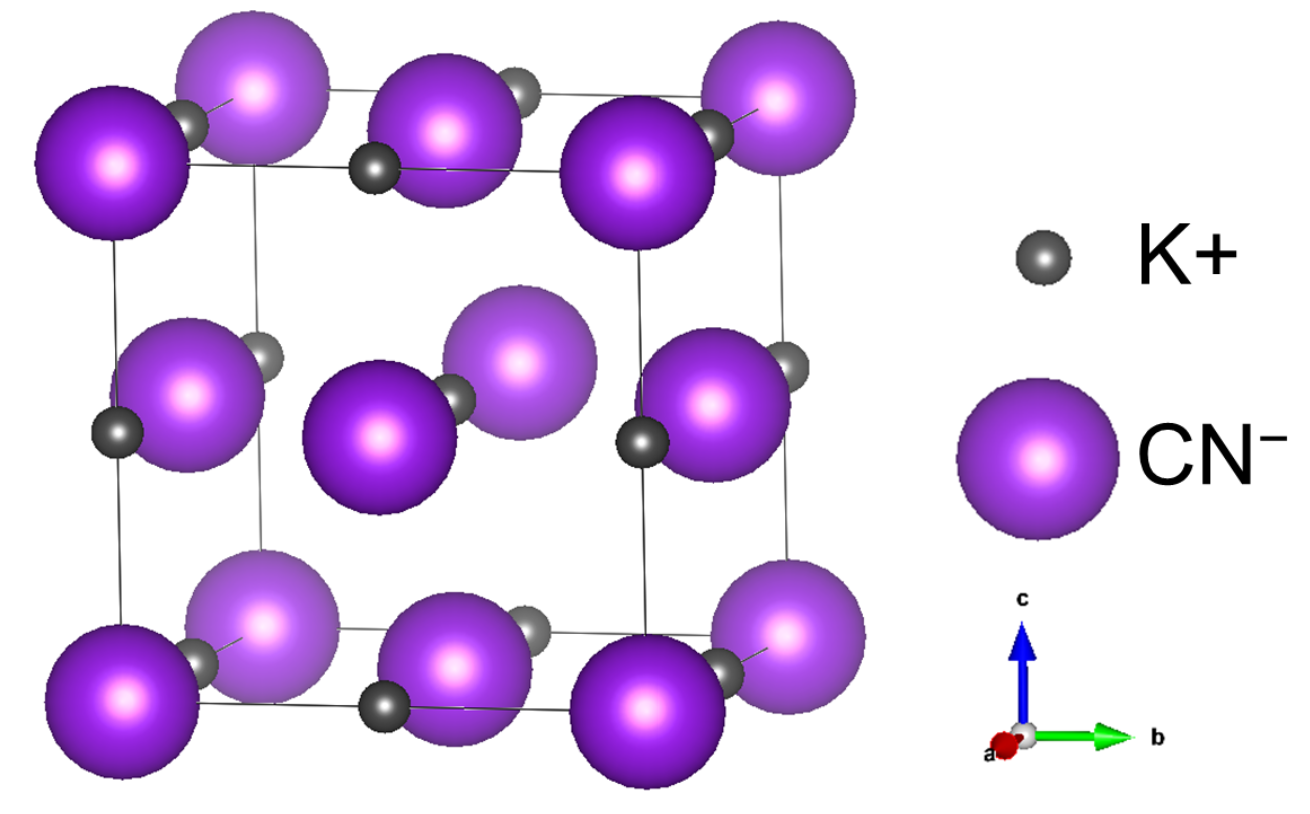
シアン化カリウムはカリウムイオンとシアン化物イオンからなるイオン結晶で、代表的なシアン化アルカリ化合物の一つです。シアン化物イオン中の炭素と窒素は三重結合で結びついています。
 白色の粉末状結晶で潮解性があり、水に良く溶け、水溶液は強アルカリ性を示します。有機溶剤(メタノール、エタノール、グリセリン)には溶けにくい特徴があります。
白色の粉末状結晶で潮解性があり、水に良く溶け、水溶液は強アルカリ性を示します。有機溶剤(メタノール、エタノール、グリセリン)には溶けにくい特徴があります。
潮解に伴って次式に従って、空気中の二酸化炭素と反応し、炭酸カリウムに変化しながらシアン化水素(HCN)を放出します。
2 KCN + H2O + CO2 → K2CO3 + 2 HCN
そのため、乾燥状態では無臭ですが、空気中ではシアン化水素による特徴的なアーモンド臭を発します。特に太陽光に当たる状態では反応が進み易いため、空気に触れないように、太陽光に当たらないように保管する必要があります。
シアン化カリウムの製法
シアン化カリウムは、シアン化水素(HCN)を水酸化カリウム(KOH)水溶液で処理し、次いで、真空中で溶液を蒸発させることによって析出させ、製造されます。
HCN + KOH → KCN + H2O
シアン化カリウムの使用用途
シアン化カリウムは、有機合成において広く用いられます。特に、ハロゲン化アルキルと反応させることで、次式に従ってニトリル(R−C≡N)を調製する反応は重要です。
R−X + KCN → R−CN + KX
工業的には、シアン化カリウムの代わりにシアン化ナトリウム(NaCN、青酸ソーダ)が使用されることも多くなってきました。
また、写真定着剤として使用されます。シアン化カリウムは、現像液中で不溶化していない銀を溶かします。これによって、画像が鮮明化・安定化して、光に敏感でなくなります。現代においては、より毒性の低い定着剤としてチオ硫酸ナトリウムが用いられることが増えています。
金や銀、銅を製錬するための薬剤としても使用されます。次式に従って、低品位の金鉱石から金を水溶性塩として浸出させます。
4 Au (s) + 8 KCN (aq) + O2 (g) + 2 H2O (l) → 4 K[Au(CN)2] (aq) + 4 KOH (aq)
同様の工程で、NaCNを使用してシアン化金ナトリウムNaAu(CN)2として浸出することもできます。
シアン化カリウムの毒性
シアン化カリウムが経口、経気道あるいは経皮により体内に入ると、細胞呼吸が強力に阻害されて、壊死します。急性シアン中毒の初期には、組織が血液中の酸素を利用できなくなるため、服毒者の顔色は赤みがかります。最も影響を受けるのは脳で、死亡の原因は低酸素脳症となります。中毒症状は、急激に進行しますので、一刻も早い処置が必要です。シアン化カリウムを摂取してから通常数分以内に症状が出ます。呼吸困難、血圧低下が生じ、意識を喪失し、やがて脳死となります。
シアン化カリウムの経口致死量は成人で200-300mgとされています。シアン化ナトリウムでの作用もシアン化カリウムと同等です。
吸い込んだ場合には、直ちに人工呼吸により新鮮な空気を肺に送り込む必要があります。経口摂取した場合には、直ちに嘔吐させ、人工呼吸を行います。