制御・計測・センシング
駆動・機械要素・電子制御部品
産業別カテゴリ
電源・エネルギー・熱処理機器
安全・保護・環境対策
材料・素材・ケミカル
電気・電子部品
構造部品・締結要素
ソフトウェア・ネットワーク
サービス
その他
全てのカテゴリ
閲覧履歴
スレオニンのメーカー19社一覧や企業ランキングを掲載中!
スレオニン (トレオニン) とは、側鎖にヒドロキシエチル基を有する必須アミノ酸の1種です。
スレオニンは人の体の中で生成できないため、食物などからの摂取が必要です。スレオニンを多く含む食物の例として、卵、鶏肉、スキムミルク、ゼラチンなどが挙げられます。
スレオニンは人のたんぱく質を構成する20種類のアミノ酸の1つで、略号はThrやTと表されます。糖原性を持っており、体内でのグルコースの生成に利用可能です。
社員数の規模
設立年の新しい会社
歴史のある会社
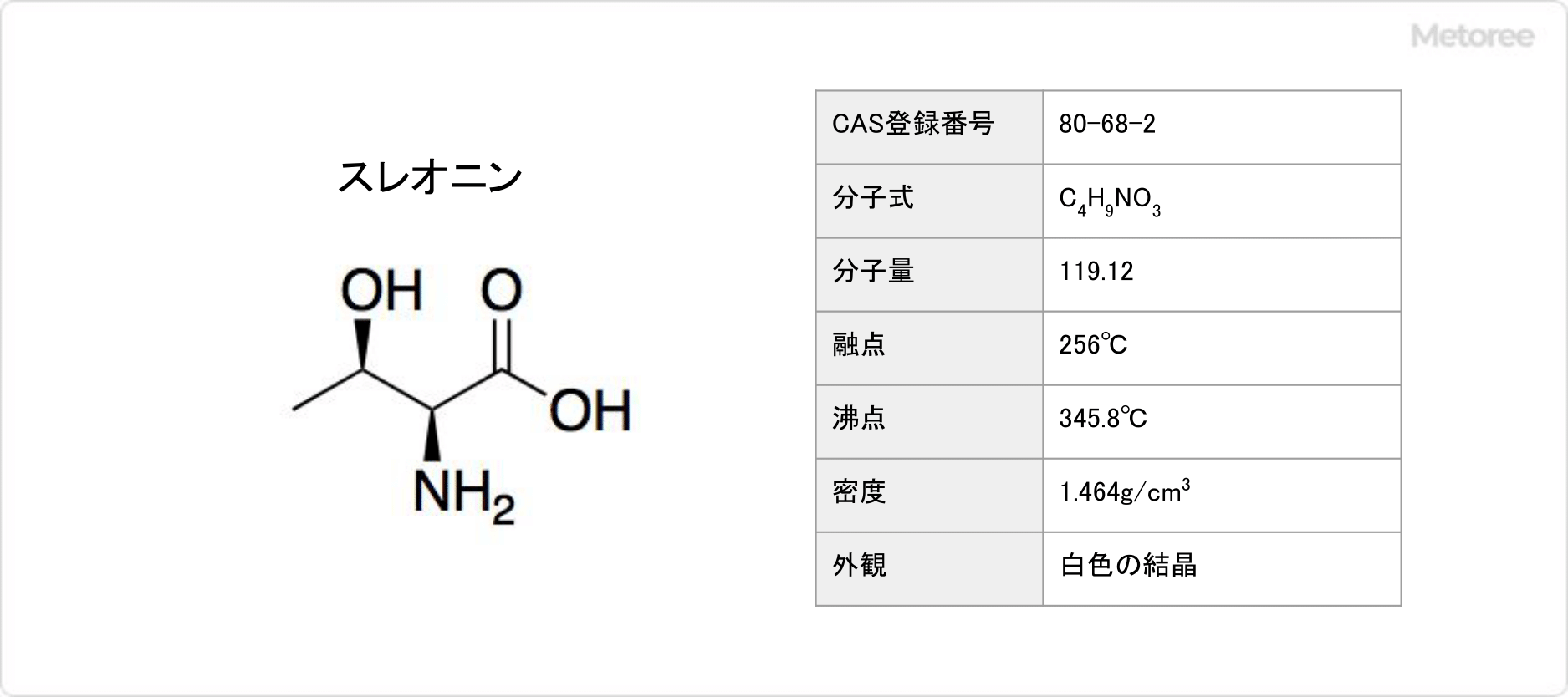
スレオニン (トレオニン) とは、側鎖にヒドロキシエチル基を有する必須アミノ酸の1種です。
スレオニンは人の体の中で生成できないため、食物などからの摂取が必要です。スレオニンを多く含む食物の例として、卵、鶏肉、スキムミルク、ゼラチンなどが挙げられます。
スレオニンは人のたんぱく質を構成する20種類のアミノ酸の1つで、略号はThrやTと表されます。糖原性を持っており、体内でのグルコースの生成に利用可能です。
スレオニンには、病気を予防する効果があります。代謝を促し、肝臓への脂肪の蓄積を防ぐため、脂肪肝を予防可能です。さらに、胃酸の分泌バランスを調整する働きがあり、胃炎を改善する効果もあります。
また、スレオニンは体内でコラーゲンを生成する際の材料です。そのため、美容効果もあり、肌の潤いを保ちます。毛髪を構成するタンパク質のケラチンを構成する要素で、髪の毛のハリや潤いを保つ効果もあります。
畜産動物にとって重要な栄養素にもなります。畜産動物の飼料にも添加されますが、餌である穀物だけでは十分な量のスレオニンを摂取できません。そこで、スレオニンなどの必須アミノ酸を添加した飼料を与えて、畜産動物の栄養バランスを保っています。
スレオニンは側鎖にヒドロキシ基を持つため、水に溶けます。カルボキシ基の酸解離定数 (pKa) は2.63で、アミノ基の酸解離定数は10.43です。
スレオニンの融点は256°C、沸点は345.8°Cです。
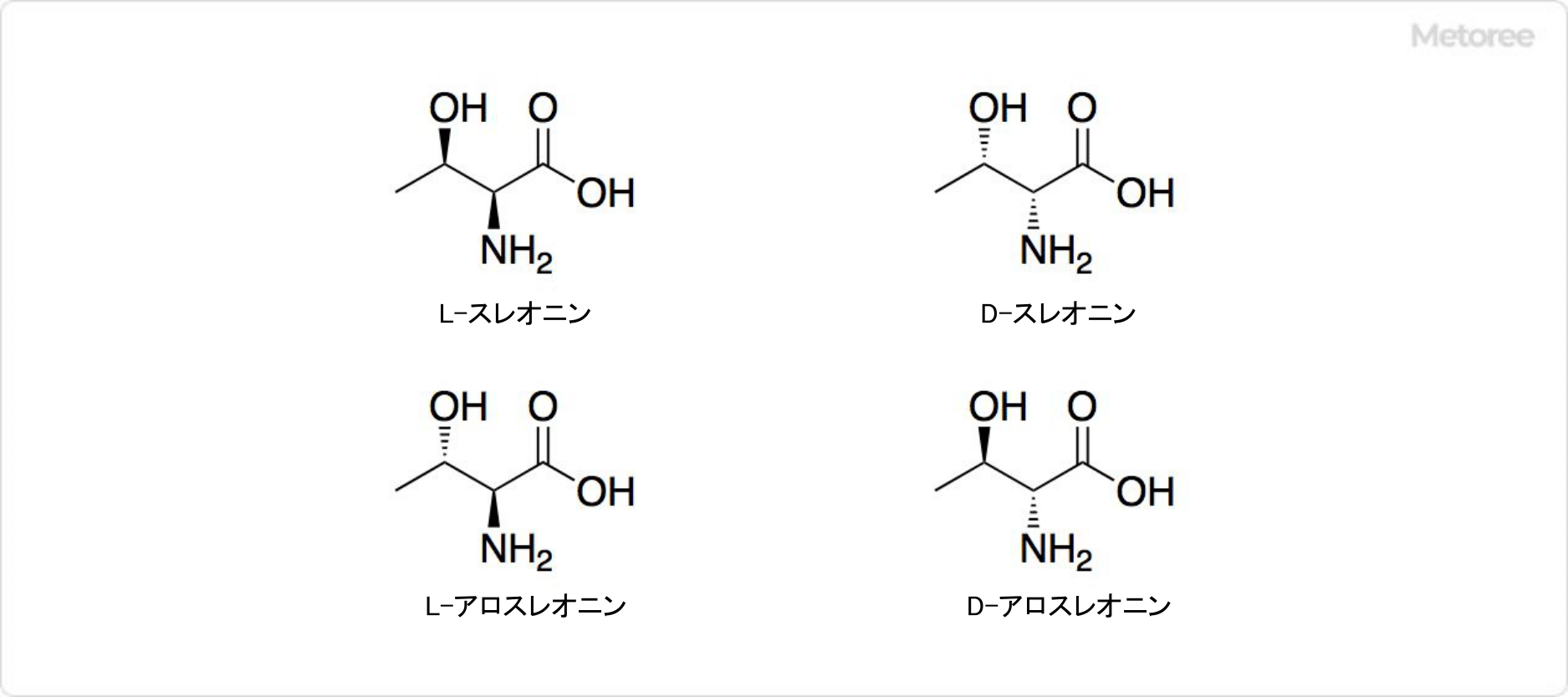
図2. スレオニンの異性体
スレオニンは四炭糖であるトレオース (英: threose) と構造が似ていたため、threonineと命名されました。極性無電荷側鎖アミノ酸に分類されています。化学式はC4H9NO3、モル質量は119.12g/molであり、密度は1.464g/cm3です。
スレオニンは2個の光学活性中心を有し、異性体が4種類存在します。つまりジアステレオマーが2種類存在します。(2S,3R)体はL-スレオニンと呼ばれ、(2S,3S)体のD-スレオニンは天然にほとんど存在しません。(2S,3S)体はL-アロスレオニン (英: L-allo-threonine) と呼ばれ、(2R,3R)体はD-アロスレオニンです。
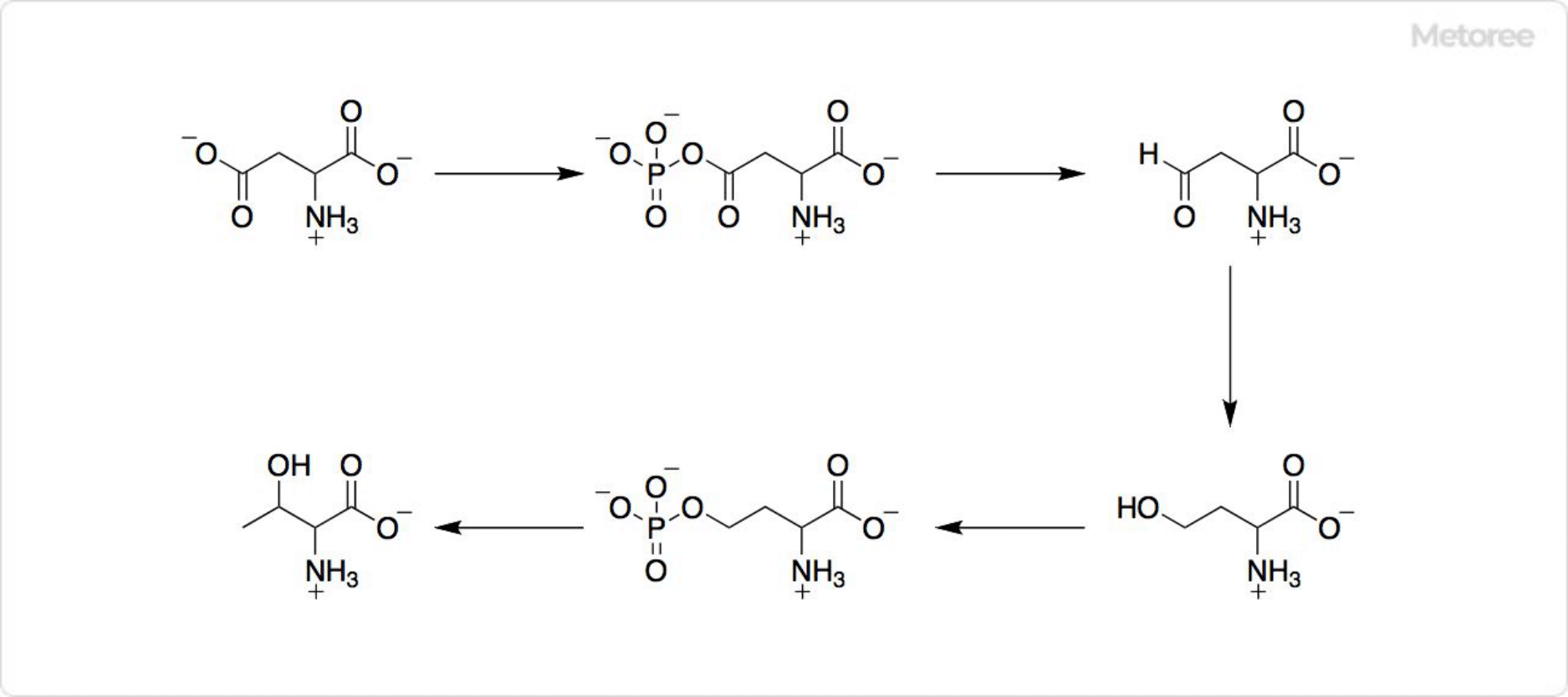
図3. スレオニンの生合成
ヒトは体内でスレオニンを合成できません。その一方で、植物や多くの微生物では、アスパラギン酸から合成可能です。
生合成ではまず、酵素のアスパルトキナーゼによってアスパラギン酸のβ-カルボキシル基がリン酸化します。続いてβ-アスパルテートセミアルデヒドデヒドロゲナーゼが還元して、β-アスパルテートセミアルデヒドが生じます。このβ-アスパルテートセミアルデヒドはスレオニン、リシン、メチオニンの生合成で重要な中間体です。
β-アスパルテートセミアルデヒドはホモセリンデヒドロゲナーゼの作用でホモセリンになり、ホモセリンキナーゼによりヒドロキシ基がリン酸化します。そしてスレオニンシンターゼによって、スレオニンが生成します。
多くの動物でスレオニンは、スレオニンデヒドロゲナーゼによってピルビン酸に変わります。CoAによる加チオール分解 (英: Thiolysis) を中間体が受けて、グリシンとアセチルCoAを生成可能です。
ラットの脳や肝臓でL-カルニチンの内因性産生中に、グリシンを合成するためにスレオニンが使用されます。ヒトでは、スレオニンはセリンデヒドラターゼによってα-ケト酪酸に変わり、スクシニルCoAになります。
多くの生物では、さらに代謝するために、キナーゼによって O-リン酸化可能です。生成物が(R)-1-アミノプロパン-2-オールに変換されて、ビタミンの側鎖に組み込まれます。これはコバラミン (ビタミンB12) の生合成の一部であり、細菌とっては重要です。