ホスフィン酸とは
ホスフィン酸とは、酸化数が1のリンのオキシ酸です。
IUPACの正式名称は、ジヒドリドジオキソリン酸 (英: dihydridodioxophosphoric acid) です。130℃以上で不均化反応が起こり、リン酸 (H3PO4) やホスフィン (PH3) になります。
強い還元性を持っているため、Cu2+やAg+などを還元できます。潮解性を有し、水・アルコール・エーテルに可溶です。25℃におけるpKaは1.244です。
ホスフィン酸の使用用途
ホスフィン酸は、有機合成用の触媒や還元剤、金属などの表面処理剤、酸化防止剤、熱変化防止剤、メッキ材料などとして、幅広く使用されています。そのほか、ホスフィン酸塩の原料も使用用途の1つです。
各種ホスフィン酸塩類は、スチールやプラスチックなどへの無電極ニッケルめっきの還元剤、各種還元や医薬品などに使用可能です。無電解ニッケルめっきの場合は、還元剤であるホスフィン酸塩が酸化されることによって、亜リン酸塩になります。この反応時に、電子を放出することで、ニッケルイオンを還元し、ニッケルとなります。
ホスフィン酸の性質
ホスフィン酸の融点は26.5℃です。100℃以上で分解し、リン化水素であるホスフィン (PH3) とホスホン酸 (PH3O3) を経て、最終的にリン酸 (H3PO4) となります。
ホスフィン酸の構造
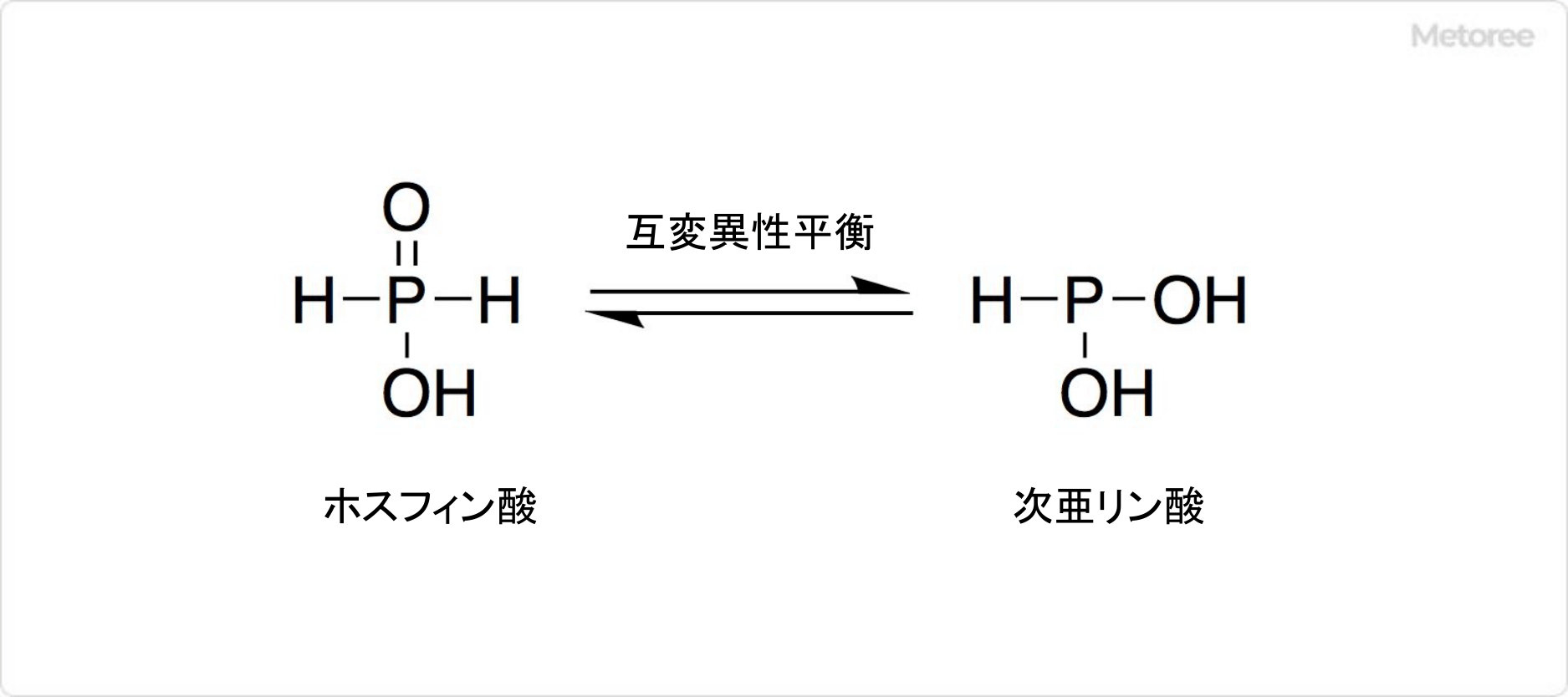
図1. ホスフィン酸の互変異性体
ホスフィン酸は、P-H結合とホスホリル基 (P=O) を有する無機リン化合物です。水素原子の2つがリンに直接結合しており、リンの原子価は5価です。式量は66.0、比重は1.45、化学式はH3PO2で、示性式は(HO)PH2(=O)で表されます。
PH2基を有することは、核磁気共鳴 (NMR) などの物理測定によって確認されています。同じ化学式の次亜リン酸と互変異性体の関係です。
ホスフィン酸のその他情報
1. ホスフィン酸の合成法
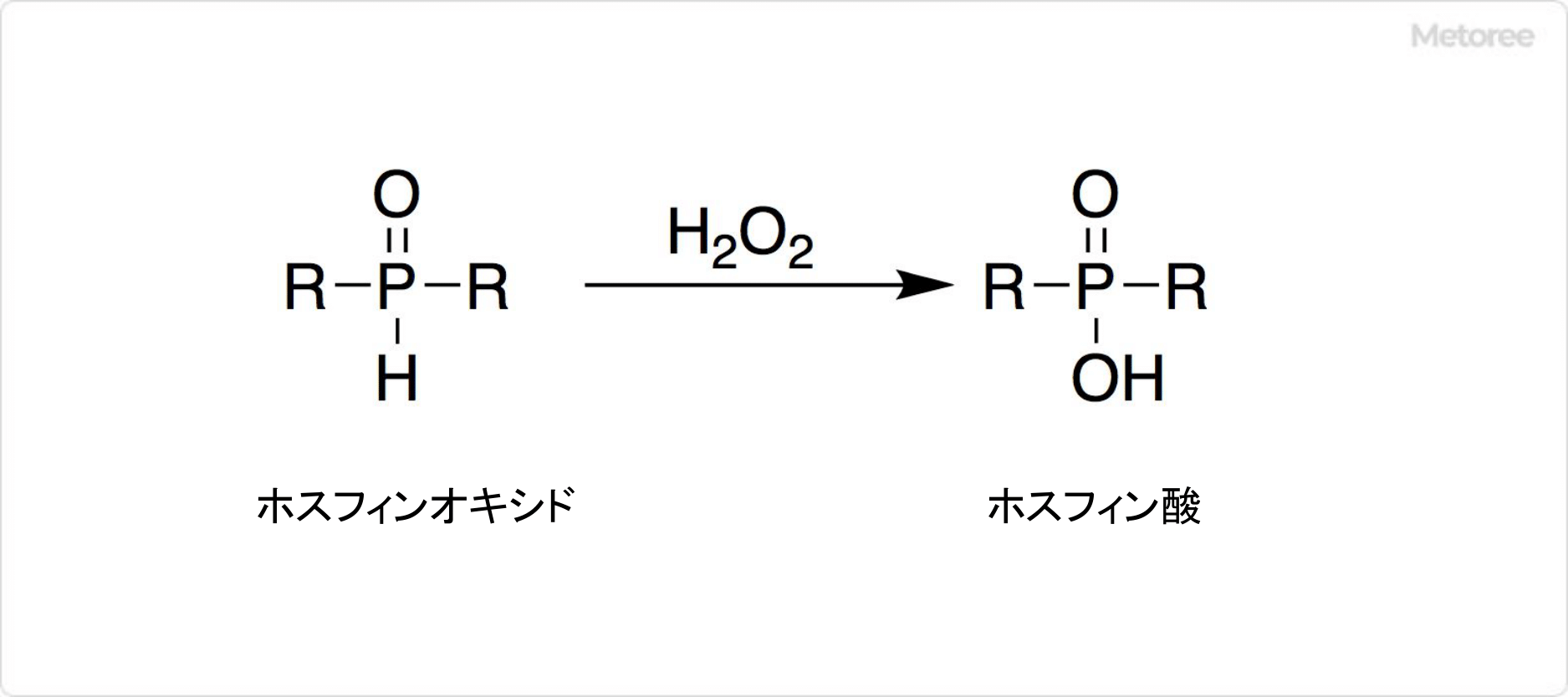
図2. ホスフィン酸の合成法
工業的にホスフィン酸を合成するために、まず白リンを消石灰で処理することによって、カルシウム塩を生成します。次に、カルシウム塩をナトリウム塩にすることで、ホスフィン酸ナトリウムが生じます。
ホスフィン酸ナトリウムをイオン交換樹脂によって酸の形に変換することで、ホスフィン酸が生成可能です。過酸化水素やヨウ素を用いて、ホスフィンオキシドを酸化する方法でも調製できます。
2. ホスフィン酸の誘導体
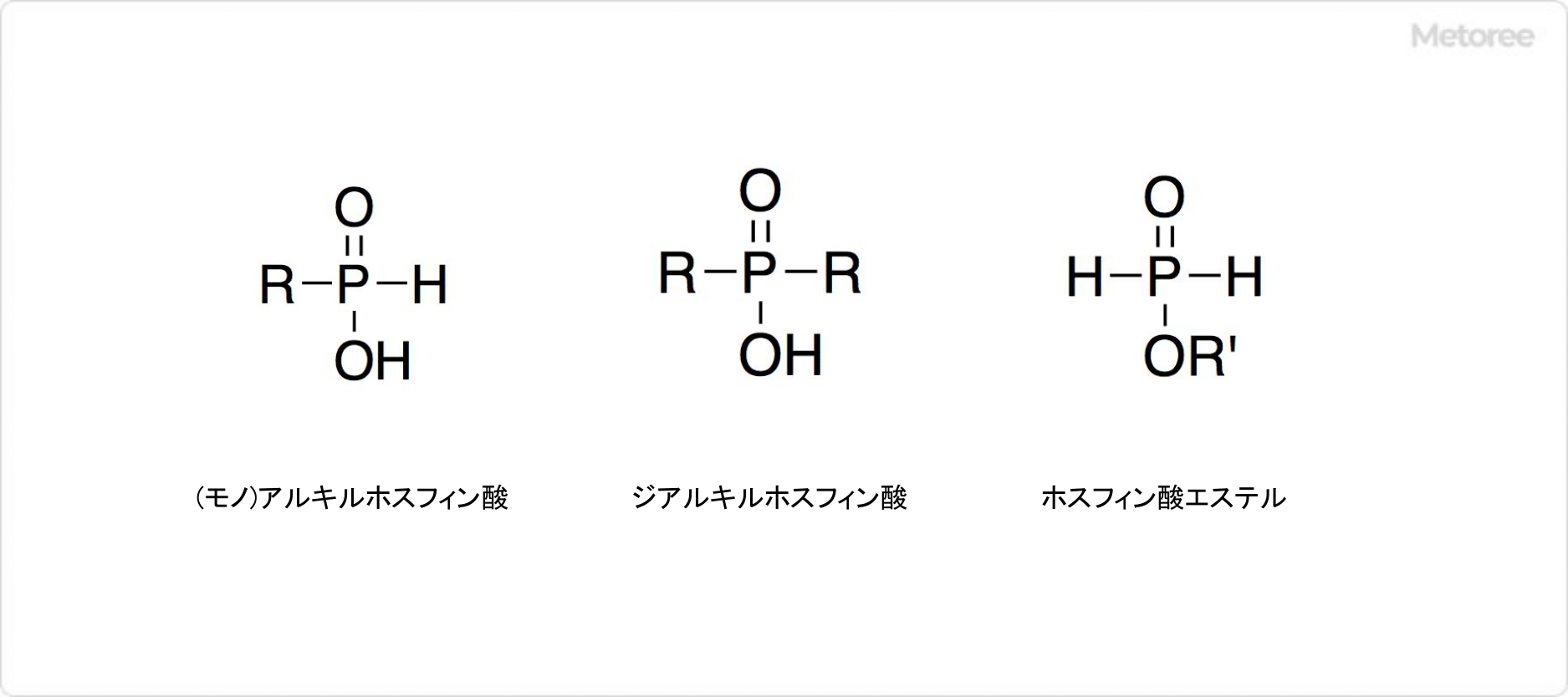
図3. ホスフィン酸の誘導体の構造
ホスフィン酸の有機誘導体には、PH基のHをアルキル基Rに置換したアルキルホスフィン酸が存在します。Rはアリール基などの有機基などです。
アルキルホスフィン酸には、PH2基のH原子のうち1つのみをアルキル基で置換されている(モノ)アルキルホスフィン酸 (RHP(O)OH) と、PH2基のH原子2つを両方ともアルキル基で置換されているジアルキルホスフィン酸 (R2P(O)OH) があります。
それ以外にも、OH基のHをアルキル基で置換したアルキルエステルも存在し、ホスフィン酸エステル (英: phosphinic ester) と呼ばれています。
3. ホスフィン酸の関連化合物
ホスフィン酸はリンのオキソ酸です。リンのオキソ酸には、リン酸 (英: phosphoric acid) 、亜リン酸 (英: phosphorous acid) 、ホスホン酸 (英: phosphonic acid) 、ペルオキソ一リン酸 (英: peroxomonophosphoric acid) があります。
リン酸の化学式はH3PO4、亜リン酸の化学式はH3PO3、ホスホン酸の化学式はH2PHO3、ペルオキソ一リン酸の化学式はH3PO5です。
リン酸のリンの酸化数は+5、亜リン酸のリンの酸化数は+3、ホスホン酸のリンの酸化数は+3、ペルオキソ一リン酸のリンの酸化数は+5です。