監修:株式会社同仁化学研究所
生化学用緩衝剤とは

緩衝液とは、酸や塩基を加えてもpHがあまり変化しない溶液をいいます。
適当な弱酸とその共役塩基の混合溶液が pH 緩衝液として利用されています。
生体成分の分離・精製や細胞培養を行なうにあたっては、溶液内の pH をー定に保つ必要があります。陸生生物の生体成分の pH は通常6.5~7.5 で、海生生物とくに海藻類は pH8 程度であるため、生化学用途としては pH6~8 の範囲を緩衝できるものでなければなりません。
1966年、Goodらは生化学用緩衝剤としての望ましい条件を考慮して、Zwitter ion 構造をもつ各種のアミノエタンスルホン酸、アミノプロパンスルホン酸誘導体を合成し、その有用性を明らかにしました。これらはGood’s bufferと呼ばれ、以下に示すような特長をもっています。
また、分子生物学研究に用いる緩衝液は、実験内容に応じてDNaseやRNaseなどbuffer中に検出されないことも必要です。
Good’s Bufferの特長
- 水に良く溶け、濃厚な緩衝液が作成できる。
- 生体膜を透過しにくい。
- 酸解離平衡が濃度、温度、イオン組成の影響を受けにくい。
- 金属イオンとの錯形成能が小さい。
- 化学的に安定で、再結晶による高純度精製が可能。
- 可視、紫外部に吸収を持たないために、目的成分の検出が容易である。
生化学用緩衝剤の使用用途
生化学用緩衝剤 (Good’s buffer) は、生体成分の分離・精製や細胞培養を行う際の培地の緩衝剤、タンパク質の精製等幅広い用途で使用されています。使用する実験系やサンプル、目的とするpHに応じて、生化学用緩衝剤 (Good’s buffer) の選択が必要となりますが、実験手法によっては適さない生化学用緩衝剤 (Good’s buffer) もありますので、注意が必要です。
生化学用緩衝剤の原理
培養細胞の特性や培養細胞を構成する生体物質における酵素による触媒反応や核酸などの化学反応は、溶解している溶液の水素イオン濃度指数 (pH) の影響を大きく受けます。そのため培養細胞溶液のpHをほぼ一定に保つことが非常に重要です。
生化学用緩衝剤はこの働きをしており、pHを一定に保つために溶液内に水素イオンを供与できる酸 (HA) とこれを受容できる共役塩基 (A–) を含有します。水素イオン濃度が減少 (pHが上昇) した時には酸であるHAが、H+とA–に解離することでpHを一定に保ち、水素イオン濃度が増加 (pHが低下) した時には共役塩基であるA–が水素イオンH+と結合して酸 (HA) となって、溶液中の水素イオン濃度 (pH) を一定に保つことが可能です。
生化学用緩衝剤(Good’s buffer)の代表的な一つであるHEPESを参考に解説します。
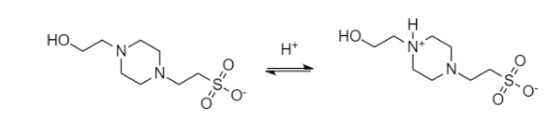
分子内のスルホン基から解離したプロトンが、ピペラジン基の4位窒素原子をプロトン化し、脱プロトン化体との平衡関係で緩衝能を示します.
生化学用緩衝剤においては、試料となる培養細胞の特性や検査内容を考慮して、培養細胞に少量の酸や塩基を追加する、あるいは希釈により濃度を変更しても影響を受けない程度の緩衝作用が必要とされます。
具体的には、陸生生物の生体成分の pH は、6.5~7.5程度であり、海生生物とくに海藻類は pH8程度であることから、生体用緩衝剤にはpH6~8の範囲を緩衝できる緩衝作用が求められています。
生化学用緩衝材のその他情報
1. 生化学用緩衝剤の利用分野
生化学用緩衝剤は、細胞試験各種の細胞試料をほぼ一定の状態で保つものです。この細胞試験には、以下のような生体への毒性を検査するものや、タンパク質の量を測定するものがあります。
- 細胞毒性試験
細胞毒性試薬は、医療機器を構成する物質や、人体に触れる化粧品などに含まれる化学物質、食品などの安全性を評価する試験です。培養細胞を用い、検査する化学物質と混在した状態で種々の条件を付加したのちに、培養細胞よりなる細胞試料内の細胞の生存率を指標として毒性を評価します。 - ELISA
ELISAは、タンパク量を測定する方法で、細胞からどれだけタンパク質が産生されたかを測定する方法です。この方法では、体の免疫機構として活躍する抗体の特性を利用してタンパク量を測定します。通常、抗体1つに対してタンパク質1つが結合するので、培養細胞にと抗体を混在させれば、タンパク質と抗体が1対1の割合で結合し、この抗体の量が分かれば細胞試料内のタンパク質の量も算出できます。 - リアルタイムPCR
リアルタイムPCRは、RNA (リボ核酸) によりわかるタンパク質のおおよその生産量を測定する方法です。生物のDNAに保持されたタンパク質の情報は、RNAを介してタンパク質となります。つまり、RNAの数はタンパク質の数と同等です。
これらの細胞検査においては、細胞試料の保存時や検査のための種々の条件を付加した際に、培養細胞が少しの環境変化や付加条件以外の環境変化で変質しないよう特性をほぼ一定に保つ必要があります。この培養細胞よりなる細胞試料の特性を一定に保つ働きをするのが、生化学用緩衝剤です。
2. 生化学用緩衝剤の種類
生化学用緩衝剤には、先程述べた緩衝作用の他に以下のような特性が求められます。
- 水への溶解性がよく、濃厚な緩衝液の作成が可能
- 試料である培養細胞の生体膜を透過しにくい
- 酸解離平衡が溶液の濃度や温度、イオン組成の影響を受けにくい
- 金属イオンと錯形成しにくい
- 化学的に安定しており、再結晶により高純度精製が可能
- 可視光、紫外線波長域に吸収を持たず、目的成分の検出を容易とする
このような特性も満たした生化学用緩衝剤としては、以下のようなものがあげられます。
- 酢酸緩衝液
酢酸緩衝液は、CH3COOHとCH3COONaにより構成されており、pH3.2-6.2の範囲の緩衝作用を持ちます。 - リン酸緩衝液
リン酸緩衝液は、NaH2PO4とNa2HPO4により構成されており、緩衝作用はpH5.2-8.3の範囲です。 - 塩化アンモニウム緩衝液
塩化アンモニウム緩衝液は、NH3とNH4Cl により構成されており、pH8.0-11.0の範囲の緩衝作用を持ちます。 - トリス緩衝液
トリス緩衝液は、H2NC(CH2OH)3 により構成されており、(HOCH2)3CNH3+ ⇆ (HOCH2)3CNH2 + H+の平衡状態を示しています。使用範囲はpH7.2~9.0です。 - HEPES緩衝液
HEPES緩衝液は、C8H18N2O4Sで構成されており、分子は両性イオンです。pH 6.8~8.2で使用されます。
このように様々な生化学用緩衝剤があります。検査する培養細胞の性質や検査項目、検査によって検出すべき特性に応じて再体用緩衝材を選択することが重要です。
参考文献
https://www.dojindo.co.jp/products/category.cgi?bid=13&code=1666923416
本記事は細胞毒性測定試薬を製造・販売する株式会社同仁化学研究所株式会社様に監修を頂きました。
株式会社同仁化学研究所の会社概要はこちら