アセチレンとは
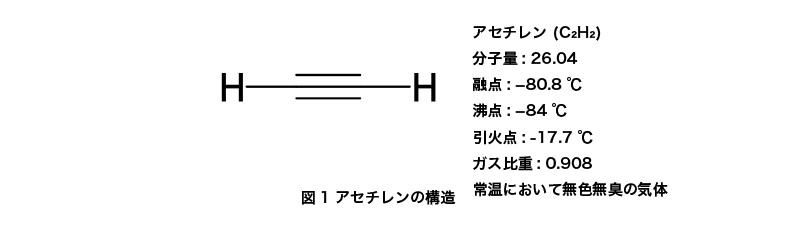
アセチレン (acetylene) とは、炭素数2の炭化水素です。
アルキン (炭素-炭素三重結合を持つ炭化水素) の中で最も単純な構造を持ち、分子式はC2H2、IUPAC系統名では「エチン」 (ethyne) と呼ばれます。常温では無色・無臭の気体であり、ガス密度は空気 (ガス密度1) よりわずかに軽く、0.908です。
天然に存在する物質ではなく、天然ガスやナフサなどの炭化水素を熱分解することで得られます。火炎温度が高く、酸素消費量も少ないことから、工業的に広く活用されている可燃性ガスです。
アセチレンの使用用途
アセチレンは、金属の溶接や溶断加工における可燃性ガスとして用いられます。火炎温度が高いことによって作業を効率的に行うことが可能で、酸素消費量が少ない故に酸素容器の使用本数を減らすことができるためです。具体的には、鉄筋の圧接、溶射やロウ付け、鉄板の切断、鋼材の焼入れなどに用いられます。
アセチレンを完全燃焼した場合の火炎温度は3,300℃にも達します。これは他の可燃性ガスと比べても非常に高い温度です。 (参考: メタンガス/2,780℃、プロパンガス/2,800℃、プロピレンガス/2,900℃、エチレンガス/3,000℃)
また、着火温度は305℃と低いため扱いやすく、更に酸素の消費量はプロパンガスの1/4ほどと、溶断ガスの中で最小です。また、反応性が高いことから、エチレン、アセトアルデヒド、ベンゼンなど、多くの有機化合物をアセチレンから合成することができます。
尚、より純度の高いアセチレンに関しては、下記のような用途があります。
- 半導体の炭素原料
- 硬質炭素膜の生成原料
- カーボンナノチューブ、カーボンナノコイルなどの新素材の合成原料
- 原子吸光分析
アセチレンの原理
アセチレンの原理を性質や合成方法、化学反応の観点から解説します。
1. アセチレンの性質
アセチレンは、化学式C2H2で表され、分子内に三重結合を一つ持ち、分子は直線形をしています。常温では水に体積比1:1の割合で溶けますが、テトラヒドロフランなどの有機溶媒により溶けやすい性質を示します。
アセチレンは、可燃性ガスとして有用である一方、極めて着火しやすく、酸素がなくても爆発的に燃焼するという性質のため、取り扱いの際は注意が必要です。滞留したアセチレンガスに着火した場合は爆発を起こすとされています。
2. アセチレンの製造方法
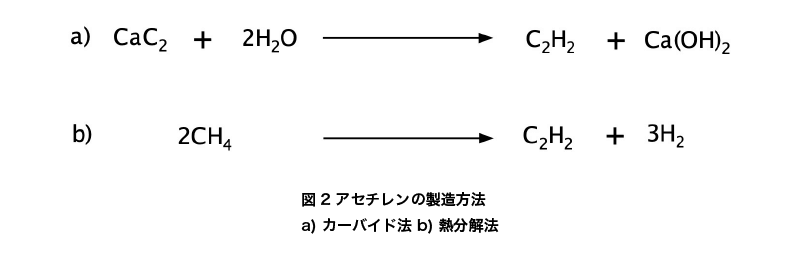
アセチレンガスの主な製造方法として、以下の2つが挙げられます。
- カーバイド法 : カーバイド(炭化カルシウム)に水を作用させる方法
- 熱分解法: 炭化水素の熱分解による方法
小規模用途ではカーバイド法によって合成され、熱分解法は大規模な工業的製造方法に限られます。ただし、工業的製造でもカーバイド法を用いることもあります。
3. アセチレンの化学反応
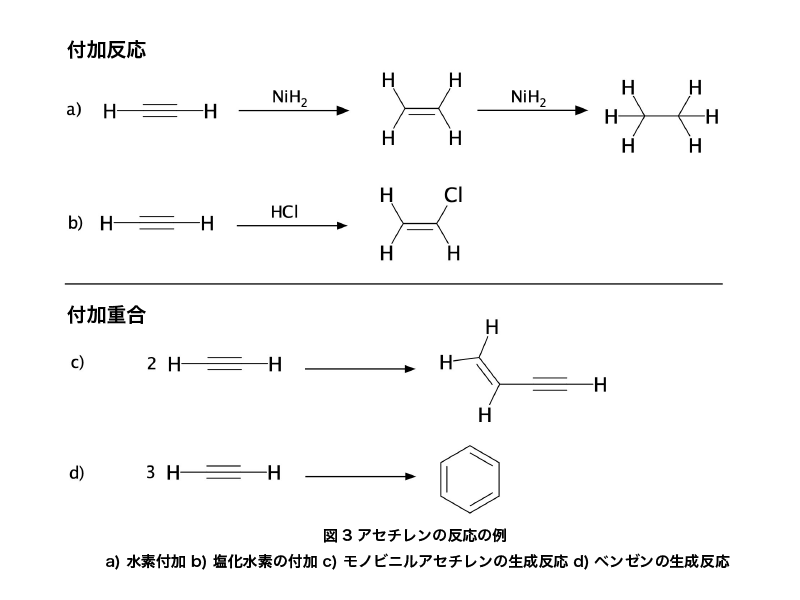
付加反応
アセチレンの三重結合は付加反応を受けやすい分子です。水素の付加によってエチレン、エタンが順に生成します。また、ハロゲン化水素などの H−X 型の分子も容易に付加反応が可能です。
付加重合
アセチレンは付加重合をすることが可能です。アセチレン2分子の重合によって、モノビニルアセチレンが生成します。モノビニルアセチレンはブタジエンやクロロプレンの原料として、合成ゴムをつくるときに用いられる物質です。また、アセチレン3分子からはベンゼンが合成されます。重合が進んでポリマー化したポリアセチレンは、導電性物質として利用されています。
アセチレンの種類
アセチレンは酸素がなくても爆発的に燃焼する危険性がある可燃性ガスです。そのため、通常は圧縮冷却により溶剤 (アセトンやDMF) などに加圧溶解させた溶解アセチレンとしてガスボンベに充填されます。
一般的な溶解アセチレンには、不純物に由来する若干の臭いがあります。これは、原材料のカルシウムカーバイドに含まれる不純物 (リン化カルシウムや硫黄など) に由来するホスフィンや硫化水素のためです。この純度のグレードの製品は、主に金属溶接・溶断加工などに使用されています。
その他には、半導体の炭素原料、硬質炭素膜の生成原料などに用いられる高純度製品などがあります。高純度アセチレンガスには、溶解アセチレンガスと、圧縮アセチレンガスがありますが、前述の通り圧縮アセチレンガスは危険性があるため取り扱いの際は注意が必要です。
尚、高圧ガス保安法により、常用の温度で圧力が0.2MPa以上になるもの、または、15℃で0.2MPa以上となるものの場合は、ボンベの色を褐色とするよう定められています。