酢酸とは
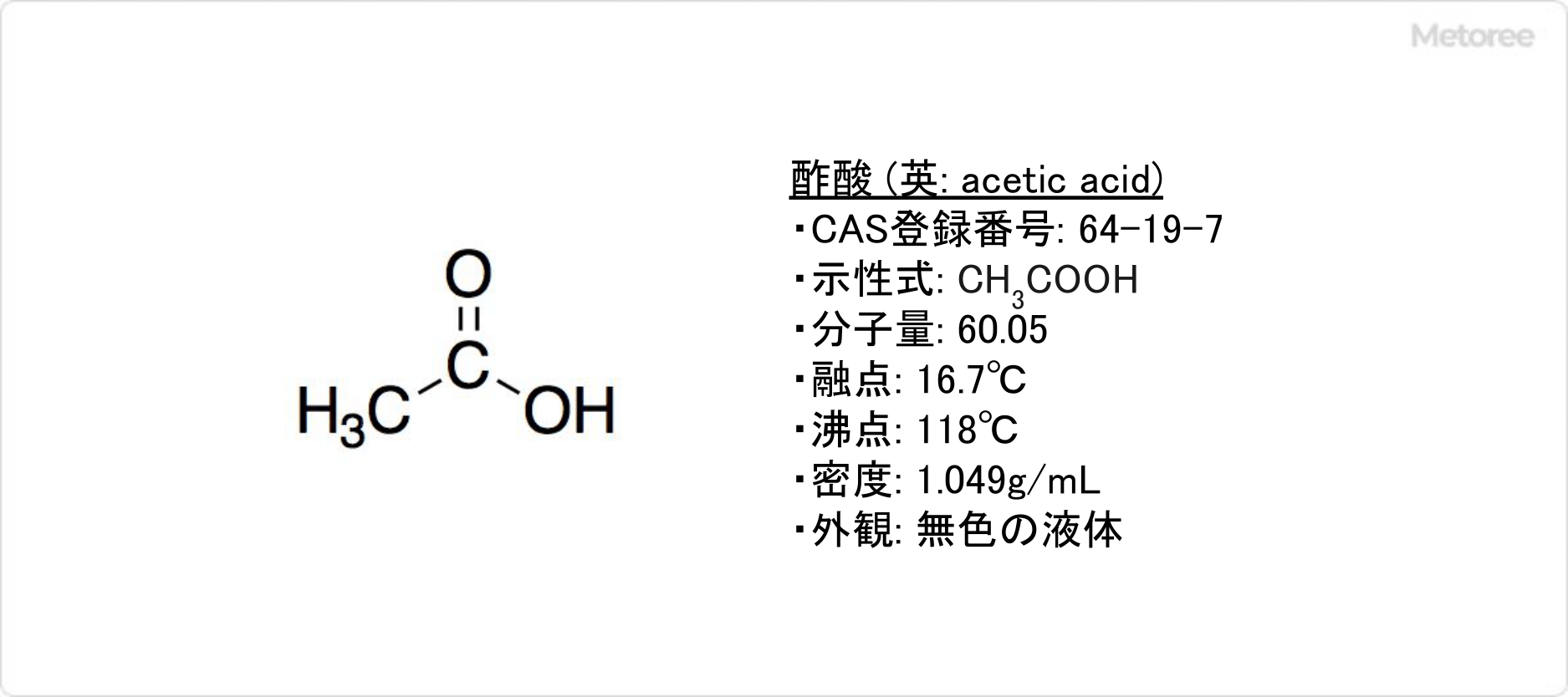
酢酸とは、酢の主成分として知られる有機化合物で、カルボン酸の一種です。
酢酸は別名、エタン酸とも呼ばれています。代表的な弱酸で、強い酸味と刺激臭がある無色透明の液体です。酢酸は、化学合成とバクテリアによる発酵 (酢酸発酵) の両方によって生成されます。
化学合成による生成の場合は、メタノールのカルボニル化によって作られることが多いです。また、酢酸は木材の乾留によって生成することもできます。
酢酸は染色や合成酢、写真の定着液等に使われています。酢酸と水との混合液は腐食性が高いため、取り扱いには注意が必要です。
酢酸の使用用途
酢酸の主な用途として、化学物質を合成するための原料が挙げられます。具体的には、酢酸ビニルや無水酢酸、アセトン、酢酸エステル、医薬品等の原料として広く用いることが可能です。
例えば、酢酸ビニルは合成樹脂の原料として、酢酸エステルは塗料の原料等として用いられています。無水酢酸は強力なアセチル化試剤であり、アセチルセルロースの製造等に用いられています。
酢酸は古くから、食酢やお漬物、ソース等の食品に、調味料や酸味料として使用可能です。また、香料の原料にも使用される等、用途は非常に幅広いです。
酢酸の性質
酢酸の融点は16.7°C、沸点は118°Cです。酢酸は水、エタノール、酢酸エチル、アセトニトリル、クロロホルム、エーテル、ベンゼンなどと任意の割合で混和します。オクタンのような長鎖炭化水素には溶けにくいです。二硫化炭素にも不溶ですが、無機塩や糖などの極性化合物は溶解します。
高純度の酢酸は低温で結晶化するため、氷酢酸と呼ばれています。2分子の酢酸が脱水縮合すると、別の化合物の無水酢酸 (英: acetic anhydride) となります。
酢酸の構造
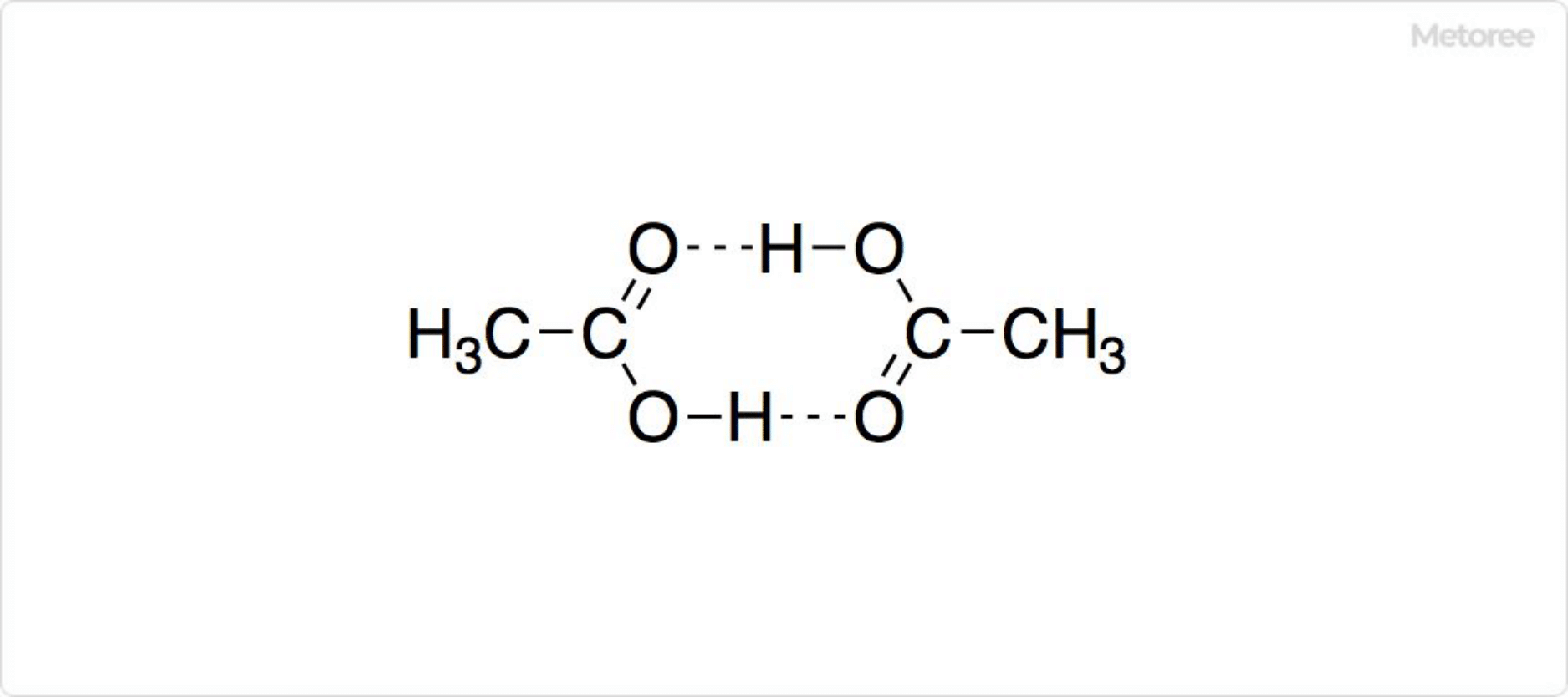
図2. 酢酸の二量体の構造
酢酸の示性式はCH3COOH、モル質量は60.05です。酢酸を構成している炭素原子と酸素原子は、同一平面上に位置しています。結合角はC−C−OHとC−C=Oが119°、O=C−OHが122°です。結合距離はC−Cが152pm、C−OHが131pm、C=Oが125pmです。
水素結合によって、酢酸2分子が結合した環状二量体を形成します。気体状態においては電子回折を用いて、固体状態においてはX線結晶構造解析を使用して、構造を確認することが可能です。
純粋な液体状態では、二量体になっているか、直鎖状や環状の多量体になっており、おそらく単量体はほとんど存在していません。ベンゼンや四塩化炭素のような非プロトン性の希薄な溶媒中では、二量体を形成します。その一方で、水のようなプロトン性の溶媒中の場合には、単量体として存在します。酢酸の沸点が比較的高い理由は、二量体を形成しているためです。
酢酸のその他情報
1. 酢酸の反応
酢酸は酸性なので、塩基との中和反応が起こります。例えば、炭酸カリウムと中和によって、酢酸カリウムを生成可能です。
酢酸は一般的なカルボン酸と同様の反応性を示します。具体的には硫酸を触媒として、アルコールとともに加熱することで、酢酸エステルを得ることが可能です。これはフィッシャーエステル合成反応 (英: Fischer esterification) と呼ばれています。フィッシャーエステル合成は可逆反応なので、効率的にエステル生成物を得るためには、過剰に出発物質を用いる必要があります。
さらに、酢酸に日光を当てて塩素と反応させると、酢酸の水素原子と塩素原子が交換されたクロロ酢酸を生成可能です。ラジカルの発生を含んだ機構で進行するため、副生成物としてジクロロ酢酸やトリクロロ酢酸も生じます。
2. 無水酢酸の合成法
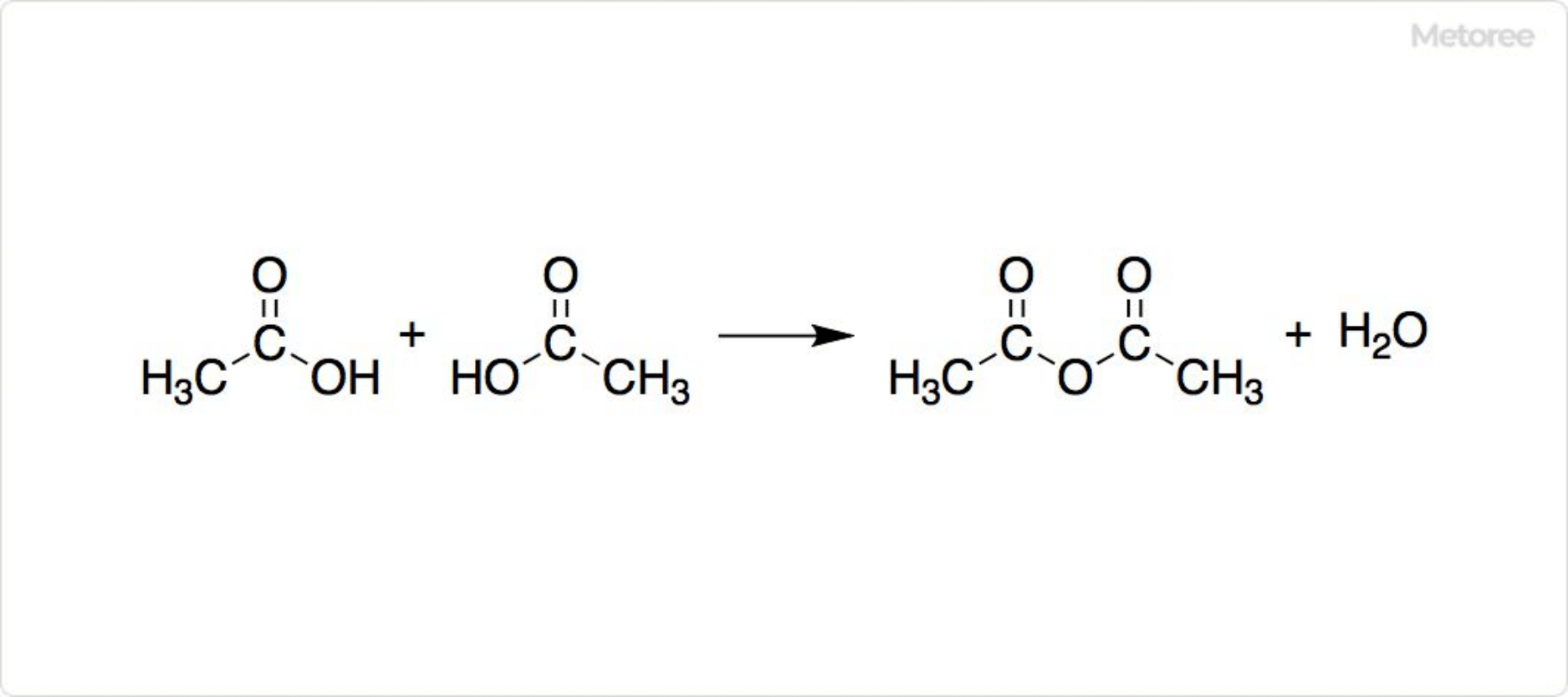
図3. 無水酢酸の合成
酢酸2分子の脱水縮合によって、無水酢酸が生成します。無水酢酸はカルボン酸無水物の一種です。無水酢酸は酢酸セルロース繊維の原料やアスピリンなどの医薬品製造のほか、香料や染料などの合成原料に用いられます。